
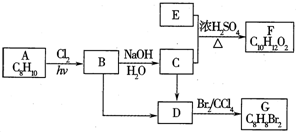
 A��G�����л���������ǵ�ת����ϵ���£�
A��G�����л���������ǵ�ת����ϵ���£�
 ��
�� ���ṹ��ʽ��
���ṹ��ʽ�� ���� E������������������ܶ�Ϊ30����Mr��E��=30��2=60��6.0gE�����ʵ�����0.1mol����ȫȼ�պ�����CO2�� H2O�����ʵ����ֱ�Ϊ$\frac{8.8g}{44g/mol}$=0.2mol��$\frac{3.6g}{18g/mol}$=0.2mol��������N��C��=$\frac{0.2mol}{0.1mol}$=2��N��H��=$\frac{0.2mol��2}{0.1mol}$=4����N��O��=$\frac{60-12��2-8}{16}$=2����E�ķ���ʽ��C2H4O2��AΪһȡ���������ɷ���ʽ��֪Ϊ����ͬϵ���AΪ ��A�������ڹ��������·���ȡ����Ӧ����B��BΪ±������B����ˮ�ⷴӦ����C��B��C��ת���õ�D���ṹG�ķ���ʽ��֪��B��C������ȥ��Ӧ����D��D�к���̼̼˫������B�к���һ��������BΪ
��A�������ڹ��������·���ȡ����Ӧ����B��BΪ±������B����ˮ�ⷴӦ����C��B��C��ת���õ�D���ṹG�ķ���ʽ��֪��B��C������ȥ��Ӧ����D��D�к���̼̼˫������B�к���һ��������BΪ ��B����ˮ�ⷴӦ����CΪ
��B����ˮ�ⷴӦ����CΪ ��C��E��Ӧ����F�����F�ķ���ʽ��֪��Ӧ�Ƿ���������Ӧ����EΪCH3COOH��FΪ
��C��E��Ӧ����F�����F�ķ���ʽ��֪��Ӧ�Ƿ���������Ӧ����EΪCH3COOH��FΪ ��B��C��������ȥ��Ӧ����DΪ
��B��C��������ȥ��Ӧ����DΪ ����GΪ
����GΪ ���ݴ˽��
���ݴ˽��
��� �⣺E������������������ܶ�Ϊ30����Mr��E��=30��2=60��6.0gE�����ʵ�����0.1mol����ȫȼ�պ�����CO2�� H2O�����ʵ����ֱ�Ϊ$\frac{8.8g}{44g/mol}$=0.2mol��$\frac{3.6g}{18g/mol}$=0.2mol��������N��C��=$\frac{0.2mol}{0.1mol}$=2��N��H��=$\frac{0.2mol��2}{0.1mol}$=4����N��O��=$\frac{60-12��2-8}{16}$=2����E�ķ���ʽ��C2H4O2��AΪһȡ���������ɷ���ʽ��֪Ϊ����ͬϵ���AΪ ��A�������ڹ��������·���ȡ����Ӧ����B��BΪ±������B����ˮ�ⷴӦ����C��B��C��ת���õ�D���ṹG�ķ���ʽ��֪��B��C������ȥ��Ӧ����D��D�к���̼̼˫������B�к���һ��������BΪ
��A�������ڹ��������·���ȡ����Ӧ����B��BΪ±������B����ˮ�ⷴӦ����C��B��C��ת���õ�D���ṹG�ķ���ʽ��֪��B��C������ȥ��Ӧ����D��D�к���̼̼˫������B�к���һ��������BΪ ��B����ˮ�ⷴӦ����CΪ
��B����ˮ�ⷴӦ����CΪ ��C��E��Ӧ����F�����F�ķ���ʽ��֪��Ӧ�Ƿ���������Ӧ����EΪCH3COOH��FΪ
��C��E��Ӧ����F�����F�ķ���ʽ��֪��Ӧ�Ƿ���������Ӧ����EΪCH3COOH��FΪ ��B��C��������ȥ��Ӧ����DΪ
��B��C��������ȥ��Ӧ����DΪ ����GΪ
����GΪ ��
��
��1��������������֪��E�ķ���ʽΪC2H4O2���ʴ�Ϊ��C2H4O2��
��2����B����C�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��3����B����D�� ������ȥ��Ӧ����
������ȥ��Ӧ���� ����Ӧ����Ϊ���������ƴ���Һ�����ȣ�
����Ӧ����Ϊ���������ƴ���Һ�����ȣ�
�ʴ�Ϊ���������ƴ���Һ�����ȣ�
��4��������������֪��F�ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5����G�� ����ͬ���칹���У�������һ�����IJ���ֻ��һ�֣����к˴Ź���������壬�ҷ������Ϊ1��1���Գ��Ըߣ����Ժ���2����ͬ��ȡ�������Ҵ��ڶ�λ���ṹ��ʽΪ
����ͬ���칹���У�������һ�����IJ���ֻ��һ�֣����к˴Ź���������壬�ҷ������Ϊ1��1���Գ��Ըߣ����Ժ���2����ͬ��ȡ�������Ҵ��ڶ�λ���ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ��ؼ���ȷ��AΪ�ұ����ٽ��ת����ϵ������ʽ�ƶϣ���Ҫѧ���������չ����ŵ�������ת�����Ѷ��еȣ�


 Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ɫ�ֱ�Ϊ��ɫ����ɫ����ɫ | |
| B�� | �������������ɫ�ֱ�Ϊ��ɫ����ɫ����ɫ | |
| C�� | ���پ��ú���Һ��Ϊ���㣬ˮ���²� | |
| D�� | ���پ��ú���Һ�Է�Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn+H2SO4�TZnSO4+H2�� | |
| B�� | C+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+2SO2��+2H2O | |
| C�� | H2S+CuSO4�TCuS��+H2SO4 | |
| D�� | S+O2$\frac{\underline{\;��ȼ\;}}{\;}$SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
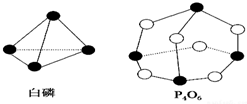 ��ѧ���ļ������γɣ���Ͽ���1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ/mol����P-P��198��P-O��360��O=O��498��������1mol P4O6����ӦP4�����ף�+3O2=P4O6�е������仯Ϊ��������
��ѧ���ļ������γɣ���Ͽ���1mol��ѧ��ʱ�ͷţ������գ�����������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJ/mol����P-P��198��P-O��360��O=O��498��������1mol P4O6����ӦP4�����ף�+3O2=P4O6�е������仯Ϊ��������| A�� | ����1638kJ���� | B�� | �ų�1638kJ���� | C�� | ����126kJ���� | D�� | �ų�126kJ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
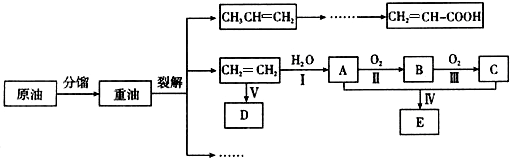
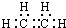 ��
��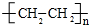 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1����2����5����6�� | B�� | ��1����4����5�� | C�� | ��2����4����6�� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
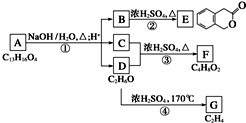 ͼ��A��B��C��D��E��F��G��Ϊ�л������������ͼ�ش����⣮
ͼ��A��B��C��D��E��F��G��Ϊ�л������������ͼ�ش����⣮ ����Ӧ�ٵķ�Ӧ������ˮ�ⷴӦ��ȡ����Ӧ����
����Ӧ�ٵķ�Ӧ������ˮ�ⷴӦ��ȡ����Ӧ����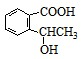 ��
��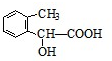 ��
��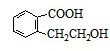 ��
�� ��CH2=CH2+H2O$��_{��}^{����}$CH3CH2OH��
��CH2=CH2+H2O$��_{��}^{����}$CH3CH2OH���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
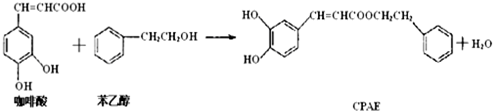
| A�� | ���������������̼ԭ�ӿ��ܴ���ͬһ��ƽ���� | |
| B�� | ���ý���Na���������Ӧ�Ƿ�������Ҵ� | |
| C�� | �뱽�Ҵ���Ϊͬ���칹��ķ������ʹ�6�� | |
| D�� | 1molCPAE��������NaOH��Һ��Ӧ���������3molNaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �屽�л����壬����KI��Һ������ֱ��������ȡ����Һ | |
| B�� | �������л���Ũ���ᣬ��������ϡNaOH��Һϴ�ӣ����÷�Һ©����Һ | |
| C�� | ��ϩ�к���SO2������ͨ��װ��KMnO4��Һ��ϴ��ƿ�н���ϴ�� | |
| D�� | �����к�����ϩ��ͨ��������H2��һ�������·�Ӧʹ��ϩת������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com