


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
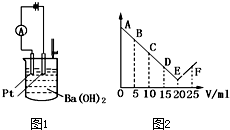 如图1所示:将30ml 0.1mol?L-1Ba(OH)2溶液置于烧杯中,然后慢慢加入0.1mol?L-1某第三周期元素形成的某酸溶液共25mL,加入酸溶液的体积V与电流强度I的I-V图如图2所示.
如图1所示:将30ml 0.1mol?L-1Ba(OH)2溶液置于烧杯中,然后慢慢加入0.1mol?L-1某第三周期元素形成的某酸溶液共25mL,加入酸溶液的体积V与电流强度I的I-V图如图2所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验操作 | 预期现象和结论 | ||
| 步骤① | 取少量待测液于试管A中,D滴加2mol?L-1HCl至溶液呈酸性,加入几滴 |
证明待测液中含SO
| ||
| 步骤② | 有白色沉淀生成证明待测液中含SO
| |||
| 步骤③ | 另取少量待测液于试管C中,加入足量氯水,再加入四氯化碳,震荡,静置后观察颜色 | 待测液中含Br- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com