
下列图示与对应的叙述不相符合的是( )
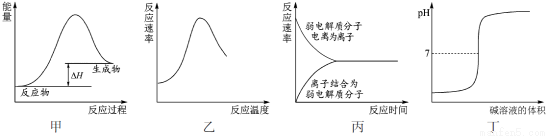
A.图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:2017届海南中学高三上第二次月考化学试卷(解析版) 题型:实验题
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3·l0H2O,为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。
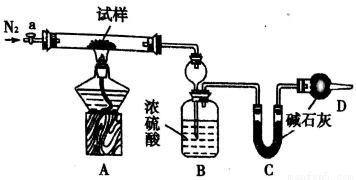
实验过程:
I.按图组装仪器,检查装置的气密性;
II.将m1 g试样放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3 g;
Ⅲ,关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;Ⅳ.称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为:________________;_______________。
(2)装置B的作用为_______________。装置C的作用为_______________。
(3)实验过程中通入N2的目的为__________。
(4)用下列各项所提供的数据能计算出NaHCO3的质量分数w(NaHCO3)的是_______(填选项字母)
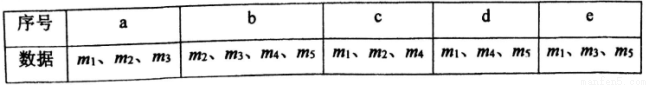
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3),若能,则w(NaHCO3)的计算式为:____________(若不能,此问不作答。)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三上第一次月考化学试卷(解析版) 题型:填空题
(1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:① ②
(2)已知离子反应:①H2A+B-=HA-+HB ②H2A+2C-=A2-+2HC则H2A、HA-、HB、HC的酸性由强到弱的排列顺序为
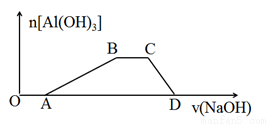
(3)向含有等物质的量浓度的HCl、NH4Cl、AlCl3混合溶液中滴加NaOH溶液,生成沉淀的物质的量随加入NaOH溶液的体积变化关系如图。试写出①OA段和②CD段发生反应的离子方程式:① ②
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三上第一次月考化学试卷(解析版) 题型:选择题
下列化合物属于有机物的是( )
A、NaCN B、CaCO3 C、CO(NH2)2 D、NH4CNO
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期调研测试化学试卷(解析版) 题型:选择题
下列实验操作能达到实验目的的是( )
实验目的 | 实验操作 | |
A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和的FeCl3溶液中 |
B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干 |
C | 比较水和乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
D | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期调研测试化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA
B.0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA
C.反应3H2(g)+N2(g)  2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
D.0.1 mol H2O2分子中含极性共价键数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源:2017届湖北省黄冈市高三上学期第一次调研化学试卷(解析版) 题型:实验题
Ba(NO3)2为无色或白色有光泽的立方晶体,微具吸湿性,有强氧化性,助燃,有毒,可用于生产烟花、信号弹、炸药、陶瓷釉药等。一种利用重晶石(BaSO4)制硝酸钡的工艺流程如下:
I.制BaS

(1)BaS溶液显碱性的原因是__________________(用离子方程式表示);
(2)重晶石与焦炭在高温锻烧时会产生一种还原性气体,此反应中氧化剂与还原剂的物质的量之比为________,每有lmol BaSO4反应,转移的电子数目为________;
II.制Ba(NO3)2
① 取340g50%精制的BaS溶液,置于装有搅拌器、温度计和导气管的三颈烧瓶中
② 在不断搅拌下,慢慢加入浓度为65%的硝酸200g,控制温度为70℃ ,并维持三颈烧瓶内大约100mmHg 的低压,反应30min,结束。请回答:
(3)反应温度控制在70℃ 左右,不宜过高的原因是____________;
(4)三颈烧瓶内维持低压的目的是__________,导出的H2S气体经NaOH溶液吸收可以获得重要的工业原材料硫化碱(Na2S), Na2S极易水解而变质,实验室配制Na2S溶液时,需在配好的溶液里加人少量的__________;
(5)依据下表中Ba(NO3)2的溶解度数据,所得溶液经_______、________,过滤、冰水洗涤、干燥后可获得纯净的Ba(NO3)2晶体。

查看答案和解析>>
科目:高中化学 来源:2017届湖北省黄冈市高三上学期第一次调研化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述中不正确的是( )
A. 100gKHCO3和CaCO3的混合物,含有的阳离子数目为NA
B.常温常压下,1 mol甲醇完全燃烧生成CO2和H2O,转移的电子数目为6NA
C.标准状况下,22.4L丙烷含有的共价键数目为10NA
D.常温下,0.1L0.1mol/L的NH4Cl溶液中,NH4+的数目为0.01NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上第一次月考化学试卷(解析版) 题型:选择题
在密闭容器中,充入SO2和18O原子组成的氧气,在一定条件下开始反应,在达到平衡后,18O存在于
A.只存在于氧气中 B.只存在于SO3中
C.只存在于SO2和SO3中 D.SO2、SO3、O2中都存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com