
| 4.48L |
| 22.4L/mol |
| . |
| M |
| m总 |
| n总 |
| 4.3g |
| 0.2mol |
|
| ||
| ||
| 1 |
| 2 |
| 1 |
| 2 |


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
 国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
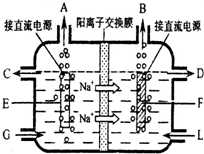 四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.
四川盛产井盐,由井盐提取的食盐是日常生活必需品,也是重要的化工原料.2- 4 |
| 加入试剂 |
| 过滤 |
| 适量盐酸 |
| 蒸发、结晶、烘干 |
2- 4 |
| ||
| ||
| ||
ρV1-
|
| ||
ρV1-
|
查看答案和解析>>
科目:高中化学 来源: 题型:


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C三种元素,已知5.75 g A单质跟盐酸完全反应,在标准状况下,可产生2.8 L(标准状况下)H2和0.25 mol ACln;B的气态氢化物的分子式是H2B,其相对分子质量与B的最高价氧化物的水化物相对分子质量比为1∶2.88,B核内质子数与中子数相等;C和B可形成CB2液态化合物,并能溶解B的单质,试完成下列问题:
(1)A、B、C的名称;A离子的结构示意图;B在周期表中的位置;CB2的分子式。
(2)用电子式表示A与B形成化合物的过程。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省井冈山市高三上学期联考化学试卷 题型:选择题
将22.4g金属粉末混合物,放入足量的稀H2SO4中至无气泡产生为止,共收集到标准状况下的H2 22.4L,此混合物可能是( )
A.锌和铜 B.镁和铁 C.铝和锂 D.锌和铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com