
����Ŀ���й����ʴ�����ͼ��ʾ��ת����ϵ(���ֲ�����ʡ��)��ͨ��CΪ���嵥�ʣ�GΪ�Ϻ�ɫ���嵥�ʡ�ʵ�����У����ù���E��B�Ĵ��¼�����ȡ���嵥��H��
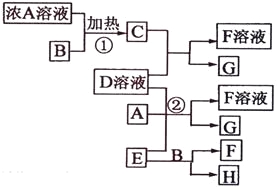
��ش��������⣺
(1)��Ӧ���Ļ�ѧ����ʽΪ_____________________
(2)��Ӧ�������ӷ���ʽΪ_____________________
(3)д������һ��ʵ������ȡH�Ļ�ѧ����ʽ____________________________
(4)D��Һ��Pb(NO3)2��Һ��Ͽ��γɳ������˳�����Ksp=7.0��10��9�����������D��Һ��Pb(NO3)2��Һ��ϣ���D��Ũ��Ϊ1��10��2mo1/L �������ɳ�������Pb(NO3)2��Һ����СŨ��Ϊ___________________��
���𰸡���Ӧ���ķ���ʽ��4HCl(Ũ) + MnO2![]() MnCl2 + Cl2�� + 2H2O ��Ӧ�������ӷ���ʽ��6I��+ ClO3-+ 6H��= 3I2+Cl��+ 3H2O 2H2O2
MnCl2 + Cl2�� + 2H2O ��Ӧ�������ӷ���ʽ��6I��+ ClO3-+ 6H��= 3I2+Cl��+ 3H2O 2H2O2![]() 2H2O + O2��(Ҳ���ø�����ؼ��ȷֽ�) D��Һ��Pb(NO3)2 ��Ӧ���ɳ���ΪPbI2��PbI2
2H2O + O2��(Ҳ���ø�����ؼ��ȷֽ�) D��Һ��Pb(NO3)2 ��Ӧ���ɳ���ΪPbI2��PbI2![]() Pb2++ 2I- ��
Pb2++ 2I- ��
Ksp= c(Pb2+)��c(I-)2= c(Pb(NO3)2 ) ��2 ��(10-2��2)2= 7.0��10-9��
����c(Pb(NO3)2 ) = 5.6��10-4mol��L-1
��������
ʵ�����У����ù���E��B�Ĵ��¼�����ȡ���嵥��H������ƶ�֪EΪ����أ�BΪ�������̣�HΪ������GΪ�Ϻ�ɫ���嵥�ʣ����ƶ�GΪ�ⵥ�ʣ�A��Ũ��Һ��B��������C�����Ƶ�C����Ϊ��������AΪ���ᣬ��ӦC��D��Һ��Ӧ����F��Һ��G����DΪ�⻯�أ�FΪ�Ȼ��أ��ݴ˴��⡣
(1)��Ӧ��Ϊʵ�����������ķ�Ӧ,��Ӧ�Ļ�ѧ����ʽΪ4HCl(Ũ) + MnO2![]() MnCl2+ Cl2�� + 2H2O��
MnCl2+ Cl2�� + 2H2O��
��ˣ�������ȷ����: 4HCl(Ũ) + MnO2![]() MnCl2+ Cl2�� + 2H2O ��
MnCl2+ Cl2�� + 2H2O ��
(2)��Ӧ��Ϊ����������������������⻯�أ���Ӧ�����ӷ���ʽΪ6I��+ ClO3-+ 6H��= 3I2+Cl��+ 3H2O��
��ˣ�������ȷ���ǣ�6I��+ ClO3-+ 6H��= 3I2+Cl��+ 3H2O��
(3)ʵ���ҿ�����˫��ˮ�ֽ�����������Ӧ�Ļ�ѧ����ʽΪ2H2O2![]() 2H2O + O2����
2H2O + O2����
��ˣ�������ȷ����: 2H2O2![]() 2H2O + O2����
2H2O + O2����
��4��D��Һ��Pb(NO3)2��Ӧ���ɳ���ΪPbI2��PbI2![]() Pb2++ 2I-��
Pb2++ 2I-��
Ksp= c(Pb2+)��c(I-)2= c(Pb(NO3)2) ��2 ��(10-2��2)2= 7.0��10-9��
����c(Pb(NO3)2) = 5.6��10-4mol��L-1��
��ˣ�������ȷ���ǣ�5.6��10-4mol��L-1��


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ͬ����ϰ����ʦ����ѧ������ϵ�д�
ͬ����ϰ����ʦ����ѧ������ϵ�д� ����ϰ�⽭��ϵ�д�
����ϰ�⽭��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ������������ԭ�����͵���
A.����ɫ��NO2����ѹ����ɫ����
B.���ڷ�Ӧ2HI(g)![]() H2 (g)��I2(g)���ﵽƽ�����С�����������ʹ��ϵ��ɫ����
H2 (g)��I2(g)���ﵽƽ�����С�����������ʹ��ϵ��ɫ����
C.ʵ�����г����ű���ʳ��ˮ�ķ����ռ�����
D.500�����ұ����¸����ںϳɰ���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ش��ȼҵ���������⣺
��1���������ռ��ǵ��ʳ��ˮʱ���չ̶��ı���k�������ȣ����ɵIJ�Ʒ��������k��_______��Ҫ��������ʽ�ͽ������
��2��ԭ�ϴ����г�������ɳ��Ca2����Mg2����Fe3����SO42�������ʣ����뾫�ƺ���ܹ����ʹ�á�����ʱ����������ˮ���˺�Ҫ������Լ��ֱ�Ϊ��Na2CO3����HCl�����ᣩ��BaCl2����3���Լ����ӵĺ���˳����______________������ţ���
��3���ȼҵ�Ǹߺ��ܲ�ҵ��һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����
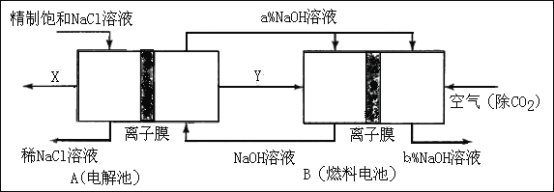
��ͼ��X��Y�ֱ���_____��_______���ѧʽ���������Ƚ�ͼʾ������������������a����b���Ĵ�С_________��
�ڷֱ�д��ȼ�ϵ��B�������������Ϸ����ĵ缫��Ӧ������______��������_____��
��������Ƶ���Ҫ�ڣ��磩��֮�����ڣ�д��2����____________��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2(g)+O2(g)![]() 2SO3(g)��Ӧ�����е������仯��ͼ��ʾ��ͼ��E1��ʾ����ʱ����Ӧ�Ļ�ܣ�E2��ʾ����ʱ�淴Ӧ�Ļ�ܣ��������й���������ȷ����
2SO3(g)��Ӧ�����е������仯��ͼ��ʾ��ͼ��E1��ʾ����ʱ����Ӧ�Ļ�ܣ�E2��ʾ����ʱ�淴Ӧ�Ļ�ܣ��������й���������ȷ����
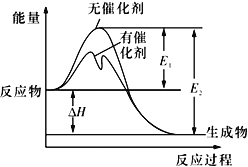
A. �÷�Ӧ���淴ӦΪ���ȷ�Ӧ�������¶ȿ������ӵİٷ���
B. 500�桢101kPa�£���1molSO2(g)��0.5molO2(g)�����ܱ������г�ַ�Ӧ����SO3(g)����akJ�����Ȼ�ѧ����ʽΪ2SO2(g)+O2(g)![]() 2SO3(g) ��H=-2a kJ��mol-l
2SO3(g) ��H=-2a kJ��mol-l
C. �÷�Ӧ�У���Ӧ����ܼ���С����������ܼ���
D. ��H=E1-E2��ʹ�ô����ı��ܣ������ı䷴Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������У� ��
�ٻ�ѧ��Ӧ���������������⣬�������������ı仯
�ڷ��ȷ�Ӧ����Ҫ���Ⱦ��ܷ���
����Ҫ���Ȳ��ܷ����ķ�Ӧ�������ȷ�Ӧ
�ܻ�ѧ��Ӧ���Ȼ������Ⱦ�������������е��������ͷ�Ӧ����е��������Ĵ�С
���Ȼ�ѧ����ʽӦע����Ӧʱ���¶���ѹǿ����ûע�����ʾ��״��ʱ�ķ�Ӧ
�����������������ֱ���ȫȼ��������̬ˮ��Һ̬ˮ��ǰ�߷ų���������
��H2(g)��I2(g)![]() 2HI(g) ��H����QkJ��mol��1��ʾ���³�ѹ�£��ں����ܱ������е���1molH2��1molI2(g)��Ӧ����2molHIʱ�ų�QkJ������
2HI(g) ��H����QkJ��mol��1��ʾ���³�ѹ�£��ں����ܱ������е���1molH2��1molI2(g)��Ӧ����2molHIʱ�ų�QkJ������
��ͬ��ͬѹ�£�H2(g)��Cl2(g)=2HCl(g)�ڹ��������º͵�ȼ�����µ���H��ͬ
A.2��B.3��C.4��D.5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����As�ǵ������ڢ�A��Ԫ�أ������γ� As2S3��As2O5��H3AsO3��H3AsO4�� ��������Ź㷺����;�ش��������⣺
��1��д�����ԭ������______________
��2����ҵ�ϳ������������Ҫ�ɷ�ΪAs2S3�Ƴɽ�״��ͨ��O2����������H3AsO4�͵�����,д��������Ӧ�Ļ�ѧ����ʽ___________;�÷�Ӧ��Ҫ�ڼ�ѹ�½��У�ԭ����___________.
��3����֪��As��s��+ ![]() H2��g��+2O2��g��=H3AsO4��s����H1
H2��g��+2O2��g��=H3AsO4��s����H1
H2��g��+![]() O2��g��=H2O��l����H2
O2��g��=H2O��l����H2
2As��s��+![]() O2��g��=As2O5��s����H3
O2��g��=As2O5��s����H3
��ӦAs2O5��s��+3H2O��l��=2H3AsO4��s���ġ�H =___________
��4��298Kʱ����20mL 3x molL-1 Na3AsO3��20mL 3x molL-1 I2��20mL NaOH��Һ��ϣ�������Ӧ��AsO33-��aq��+I2��aq��+2OH-AsO43-��aq��+2I-��aq��+H2O��l������Һ��c��AsO43-���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ��
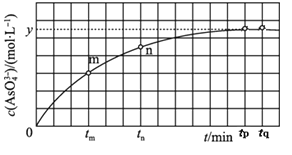
�����п��жϷ�Ӧ�ﵽƽ����� ______ ���ţ�
a .��Һ��pH���ٱ仯 b. v��I-��=2v��AsO33-��
c .c ��AsO43-��/c ��AsO33-�����ٱ仯 d. c��I-��=ymolL-1
��tmʱv��_____v��������ڡ���С�ڡ����ڡ�����
��tmʱv��_____ tnʱv��������ڡ���С�ڡ����ڡ��������� _____
����ƽ��ʱ��Һc(OH-)=1 mol/L����÷�Ӧ��ƽ�ⳣ��KΪ ______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��PCMX��һ�ְ�ȫ����Ч�����ķ�ùɱ�������ѹ㷺Ӧ���ں�Ƥ���Ӵ��ĸ��˻�����Ʒ��ϴ��Һ��������ȥм�㲨�Ȳ�Ʒ�У���ɱ���²�������ŧ���²��������²��Խ�ĸ���ȡ�����ӽṹ��ͼ��ʾ������PCMX����������ȷ���ǣ� ��
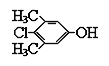
A.���������ڷ������ʣ�������ˮ
B.�������ڳ���������ɫ���壬����ʽΪC8H6ClO
C.�����ʲ��ܳ��ڸ�Ƥ���Ӵ����������Ϻ�Ӧ����ϴ��
D.�����£�1mol������������NaOH��Һ��ȫ��Ӧ����NaOH 2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ����PCl5���ȼ��ӷ��������ֽ⣺PCl5(g)![]() PCl3(g)��Cl2(g)���ֽ�5.84 g PCl5װ��2.05 L����ܱ������У���277 ��ﵽƽ�⣬������ѹǿΪ1.01��105Pa���������֪ƽ��ʱ�����ڻ����������ʵ���Ϊ0.05 mol����ƽ��ʱPCl5�ķֽ���__________��
PCl3(g)��Cl2(g)���ֽ�5.84 g PCl5װ��2.05 L����ܱ������У���277 ��ﵽƽ�⣬������ѹǿΪ1.01��105Pa���������֪ƽ��ʱ�����ڻ����������ʵ���Ϊ0.05 mol����ƽ��ʱPCl5�ķֽ���__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ����������о���Ա������ú��������Ȼ�ѧѭ��ʵ��̫���ܵ�ת����洢���������£�
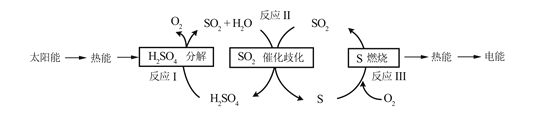
��1����Ӧ��2H2SO4(l)![]() 2SO2(g)+2H2O(g)+O2(g) ��H1=+551 kJ��mol��1
2SO2(g)+2H2O(g)+O2(g) ��H1=+551 kJ��mol��1
��Ӧ��S(s)+O2(g)![]() SO2(g) ��H3=��297 kJ��mol��1
SO2(g) ��H3=��297 kJ��mol��1
��Ӧ����Ȼ�ѧ����ʽ��________________��
��2���Է�Ӧ����ijһͶ�ϱ�ʱ������ѹǿ�£�H2SO4��ƽ����ϵ�����ʵ����������¶ȵı仯��ϵ��ͼ��ʾ��
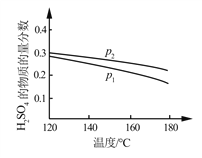
p2_______p 1����������������ó��ý��۵�������________________��
��3��I��������Ϊˮ��Һ��SO2�绯��Ӧ�Ĵ��������ܵĴ��������¡���ii����������
i��SO2+4I��+4H+![]() S��+2I2+2H2O
S��+2I2+2H2O
ii��I2+2H2O+_________![]() _________+_______+2 I��
_________+_______+2 I��
��4��̽��i��ii��Ӧ������SO2�绯��Ӧ���ʵĹ�ϵ��ʵ�����£��ֱ�18 mL SO2������Һ���뵽2 mL�����Լ��У��ܱշ��ù۲�������֪��I2���ܽ���KI��Һ�У�
��� | A | B | C | D |
�Լ���� | 0.4 mol��L��1 KI | a mol��L��1 KI 0.2 mol��L��1 H2SO4 | 0.2 mol��L��1 H2SO4 | 0.2 mol��L��1 KI 0.0002 mol I2 |
ʵ������ | ��Һ��ƣ�һ��ʱ�����ֻ��� | ��Һ��ƣ����ֻ��ǽ�A�� | ���������� | ��Һ���غ�ɫ�ܿ���ɫ����ɻ�ɫ�����ֻ��ǽ�A�� |
��B��A�ĶԱ�ʵ�飬��a=__________��
�ڱȽ�A��B��C���ɵó��Ľ�����______________________��
��ʵ�������SO2���绯��Ӧ����D��A�����i��ii��Ӧ���ʽ���ԭ��________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com