
【题目】利用“五室电渗析法”处理含硫酸钠废水的原理如图所示,以石墨为电极材料,室与室之间用离子交换膜分开(阳膜和阴膜分别只允许阳离子、阴离子通过),下列说法不正确的是 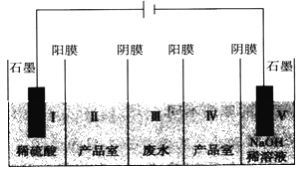
A. 阳极反应式为2H2O-4e-==O2↑+4H+,发生氧化反应
B. 通电片刻后,I、III、V室的pH依次减小、不变、增大
C. 当电路中通过1mol电子时,有1molSO42-从III室进入Ⅱ室
D. 总反应式为Na2SO4+4H2O![]() 2NaOH+H2SO4+O2↑+2H2↑
2NaOH+H2SO4+O2↑+2H2↑
【答案】C
【解析】A. 阳极上溶液中的水放电,发生氧化反应,电极反应式为2H2O-4e-=O2↑+4H+,故A正确;B. 通电片刻后,I中生成氢离子,溶液的pH减小;III中的阴阳离子分别向Ⅱ和Ⅳ移动,硫酸钠的浓度减小,溶液仍呈中性,pH不变;V室中阴极上溶液中的水放电,发生还原反应,2H2O+2e- = H2↑+ 2OH―,溶液的pH增大,故B正确;C. 根据得失电子守恒和溶液的电荷守恒,当电路中通过1mol电子时,有0.5molSO42-从III室进入Ⅱ室,故C错误;D. 根据A和B的分析,该电解装置的总反应式为Na2SO4+4H2O![]() 2NaOH+H2SO4+O2↑+2H2↑,故D正确;故选C。
2NaOH+H2SO4+O2↑+2H2↑,故D正确;故选C。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
【题目】由下列实验及现象得出的结论正确的是
实验 | 现象 | 结论 | |
A | SO2与H2S气体混合 | 产生淡黄色沉淀 | 氧化性:SO2>S |
B | 向盛有FeSO4溶液的试管中滴入氯水,然后滴入KSCN溶液 | 滴入KSCN后溶液变为红色 | 原FeSO4溶液已被空气中O2氧化变质 |
C | 试管中盛有Cu(NO3)2溶液,底部有少量铜,向其中加入稀硫酸 | 铜粉逐渐溶解 | 铜可与稀硫酸反应 |
D | 向2支盛有2mL相同浓度的NaOH溶液的试管中分别滴入2滴相同浓度的AlCl3和MgCl2溶液,振荡并静置 | 前者无沉淀,后者有白色沉淀 | Ksp[Al(OH)3]>Ksp[Mg(OH)2] |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)反应Cl2+H2OH++Cl-+HC1O其化学平衡常数的K表达式为:_________
(2)常温下,向一定体积的0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是______
A.溶液中导电粒子的数目减少
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中 不变
不变
D.溶液中 减小
减小
(3)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离.但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4=H++HSO4-,HSO4-H++SO42-.
请据此回答下列有关问题:
①Na2SO4溶液呈______(填“弱酸性”、“中性”或“弱碱性”).
②写出下列反应的离子方程式
H2SO4溶液与BaCl2溶液反应______;
H2SO4溶液与Na2SO4溶液反应______.
③在0.1molL-1的Na2SO4溶液中,下列粒子浓度关系式正确的是______.(填编号)
A.c(SO42-)+c(HSO4-)=0.1molL-1
B.c(SO42-)+c(HSO4-)=2c(Na+)
C.c(OH-)=c(H+)+c(HSO4-)
D.c(Na+)+c(H+)=c(OH-)+c(HSO4-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高中化学兴趣小组设计合成高分子材料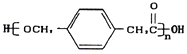
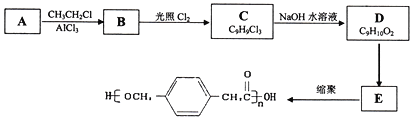
已知:
①A的相对分子质量为92;
②根据结构分析得知同一碳原子上连接两个羟基时结构不稳定,易脱水生成醛或酮;
③D可与新制的氢氧化铜反应;
回答下列问题:
(1)A的结构简式为:___________,B的名称为___________,由B生成C的反应类型是:___________。
(2) 由C生成D的化学方程式为:____________________________,反应过程中生成不稳定的中间产物结构简式为:___________。
(3)写出D转化为E的流程示意图:___________ (示例![]() )
)
(4)E合成高分子材料的化学反应方程式:_________________________________。
(5)E的同分异构体中,满足下列条件的有___________种。
①仅含有苯环,无其他环状结构;
②苯环上只有两个取代基;
③能使三氯化铁溶液显紫色;
④ 含有![]() 的结构;
的结构;
其中核磁共振氢谱表明分子中有六种氢,能发生银镜反应且其峰面积之比为2∶2∶2∶2∶1∶1
请写出其结构简式为:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质:①金刚石和石墨; ②H、D和T;③苯和乙苯;④CH3(CH2)2CH3和(CH3)2CHCH3中,互为同位素的是(填序号,下同) , 互为同素异形体的是 , 互为同系物的是 , 属于同分异构体的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,体积均为1L的HA、HB的两种一元酸溶液,分别向其中加水稀释至体积V,pH随lgV的变化关系如图所示。下列说法正确的是
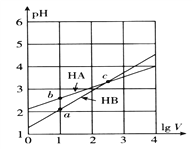
A. HA是弱酸,HB是强酸
B. 相同温度、相同浓度的NaA、NaB溶液的pH,后者大
C. c点处,分别加入足量的锌粒,HA中产生氢气多
D. a、b、c三点,由水电离出来的c(H+)·c(OH-)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学要在奥运五连环中填入物质,使相连物质间能发生反应,不相连物质间不能发生反应。你认为“五连环”中有空缺的一环应填入的物质是( )

A. 硫酸 B. 氧气 C. 二氧化碳 D. 氧化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Zn(s)+![]() O2(g)=ZnO(s)ΔH=-348.3kJ·mol-1
O2(g)=ZnO(s)ΔH=-348.3kJ·mol-1
②2Ag(s)+![]() O2(g)=Ag2O(s)ΔH=-31.0kJ·mol-1
O2(g)=Ag2O(s)ΔH=-31.0kJ·mol-1
则Zn与Ag2O反应生成ZnO和Ag的热化学方程式为
A. 2Zn(s)+2Ag2O(s)===2ZnO(s)+4Ag(s)ΔH=-634.6 kJ·mol-1
B. Zn+Ag2O===ZnO+2Ag ΔH=+317.3kJ·mol-1
C. Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)ΔH=-317.3kJ
D. Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)ΔH=+317.3kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com