
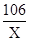 =
=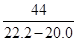
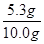 ×100%=53.0%;
×100%=53.0%;

科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.③④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同条件下,在水中的溶解性:碳酸钠 < 碳酸氢钠 |
| B.相同条件下,热稳定性:碳酸钠 > 碳酸氢钠 |
| C.相同条件下,与酸反应的速率:碳酸钠 > 碳酸氢钠 |
| D.一定条件下,碳酸钠不能转化为碳酸氢钠,而碳酸氢钠可以转化为碳酸钠 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
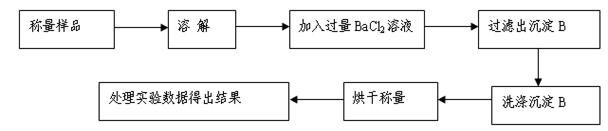
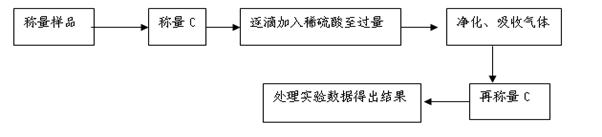

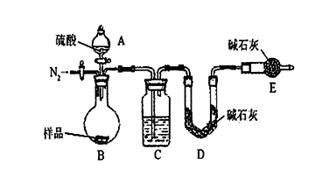
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液中c(CO32-):c(HCO3-)<1:2 |
| B.溶液中c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
| C.向混合液中滴加少量稀盐酸或NaOH溶液,HCO3-的物质的量均会减少 |
| D.将混合液蒸干,水解加剧,最终得NaOH固体 |
查看答案和解析>>
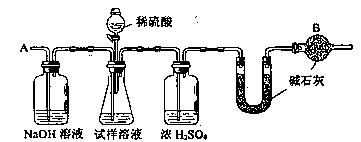
科目:高中化学 来源:不详 题型:实验题
| 步骤一:取少量制品于试管中,加少量蒸馏水,振荡,溶解。往试管中加入 振荡,观察 | 现象:溶液中产生大量白色沉淀; 结论: 。 |
| 步骤二:将步骤一的浊液过滤,取滤液于试管中B中,加入 , 振荡,观察 | 现象: ; 结论:样品中含有NaHCO3。 |
| 步骤三:将步骤二的浊液过滤,取滤液于试管C中, 振荡,观察 | 现象: ; 结论: 。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com