
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,17g甲基(-14CH3)所含的中子数为9NA
B.标准状况下, 11.2L苯中含有的碳碳双键数为1.5NA
11.2L苯中含有的碳碳双键数为1.5NA
C.42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA
D.5.6g铁与0.1mol氯 气在点燃条件下充分反应,转移的电子数为0.3NA
气在点燃条件下充分反应,转移的电子数为0.3NA
科目:高中化学 来源: 题型:
金属冶炼与处理常涉及氧化还原反应。
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2===4CuSO4+2H2O,该反应的还原剂是________。当1 mol O2发生反应时,还原剂所失电子的物质的量为________ mol。向CuSO4溶液中加入镁条时有气体生成,该气体是________。
(3)
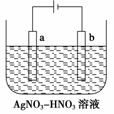
右图为电解精炼银的示意图,________(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为________。
(4)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,使Ag2S转化为Ag,食盐水的作用是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量小苏打样品(含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果____________。(选填“偏高”、“偏低”或“不受影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,在0.2mol/L Al2(SO4)3溶液中,逐滴加入1.0mol/L NaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:
Al3+ + 3OH-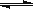 Al(OH)3
Al(OH)3
B.a-b段,溶液pH增大,Al3+浓度不变
C.b-c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的叙述正确的是
A.粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强
B.SiO2既能溶于NaOH溶液又能溶于HF溶液,说明SiO2是两性氧化物
C.乙烯能使溴水、酸性高锰酸钾溶液褪色,说明乙烯具有漂白性
D.铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,因为铁钉表面形成了一层致密稳定的氧化膜
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如右图所示。下列有关溶液中离子浓度关系叙述正确的是
 A.W点所示的溶液中:
A.W点所示的溶液中:
c(Na+)+ c(H+)=2c(CO32-)+ c(OH-)+ c(Cl-)
B.pH=4的溶液中:
c(H2CO3)+ c(HCO3-)+ c(CO32-)<0.1 mol·L-1
C.pH=8的溶液中:
c(H+)+ c(H2CO3)+ c(HCO3-) = c(OH-)+c(Cl-)
D.pH=11的溶液中:
c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:A、B、C、D、E是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2P轨道 上只有两个电子, C元素的基态原子L层只有2对成对电子,D元素在第三周期元素中电负性最大,E2+的核外电子排布和Ar原子相同。
上只有两个电子, C元素的基态原子L层只有2对成对电子,D元素在第三周期元素中电负性最大,E2+的核外电子排布和Ar原子相同。
请回答下 列问题:
列问题:
(1)分子式为BC2的空间构型为 ;D元素原子的核外电子排布式为  。
。
(2)B第一电离能比C__________(填“大”或“小”);A与B形成的最简单化合物的分子空间构型为___ _____________,其中心原子的杂化为 。
_____________,其中心原子的杂化为 。
(3)A2C所形成的晶体类型为 ;E单质所形成的晶体类型为_______。
(4)若向由A、C组成某种化合物的稀溶液中加入少量二氧化锰,有无色气体生成。则该化合物的分子 式是 ,属于 分子(填:“极性”或“非极性”),该反应的化学方程式是:_________________ __________。
式是 ,属于 分子(填:“极性”或“非极性”),该反应的化学方程式是:_________________ __________。
(5)C跟E可形成离子化合物,其晶胞结构与NaCl的晶胞相似,同为面心立方结构。该离子化合物晶体的密度为ρg·cm-3,NA表示阿伏加德罗常数,则该离子化合物晶胞的体积是 (用含ρ、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列化学方程式的配平
⑴ KMnO4+ KNO2+囗____── MnSO4+ K2SO4+ KNO3+ H2O
⑵ ClO-+ Fe(OH)3+囗____── Cl-+ FeO42-+ H2O
⑶3Pt+4HNO3+18HCl——3H2PtCl6+4NO↑+囗____
⑷ Na+ H2O── Na++ OH-+ H2↑
⑸ CrO3(红色)+ C2H6O(乙醇)+ H2SO4── Cr2(SO4)3(绿色)+ C2H4O(乙醛)+ H2O
⑹ Cu2S+ HNO3(稀)- Cu(NO3)2+ H2SO4+ NO↑+ H2O
⑺ Na2O2+ CO2── Na2CO3+ O2
⑻ NH4NO3── HNO3+ N2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为____________。
(2)写出该反应的化学方程式_________________________________________________。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现.你判断该气体泄漏时的现象是
。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有__________________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com