
下列说法正确的是( )
A.摩尔是一个国际基本物理量
B.标准状况下气体摩尔体积约为22.4 L
C.1 mol氧的质量为16 g
D.1 mol CO2的质量以克为单位时,在数值上等于CO2的相对分子质量
科目:高中化学 来源: 题型:
(1) 常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入 0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
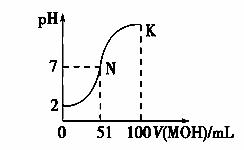
①由图中信息可知HA为________(填“强”或“弱”),理由是___________。
②常温下一定浓度的MA稀溶液的pH=a,则a________7(填“>”、“<”或“=”)。
③请写出K点所对应的溶液中离子浓度的大小关系: 。
(2)已知25 ℃时0.1 mol·L-1醋酸溶液的pH约为3,向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,增大了c(OH-),因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
①为了验证上述哪种解释正确,做如下实验:向0.1 mol·L-1的醋酸溶液中加入少量下列物质中的________(填写编号),然后测定溶液的pH。
A.固体CH3COOK B.固体CH3COONH4
C.气体NH3 D.固体NaHCO3
②若乙的解释正确,溶液的pH应________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C三种化合物,各取40 g相混合,完全反应后,得到18 g B、49 g C,还有D生成。已知D的相对分子质量为106。现将22 g A和11 g B反应,能生成D的物质的量是( )
A.1 mol B.0.5 mol
C.0.275 mol D.0.25 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
浓度为2 mol·L-1的NaOH溶液的正确含义是( )
A.在2 L水中溶有80 g NaOH B.80 g NaOH溶于水配成的溶液
C.1 L溶液中溶有80 g NaOH D.2 L溶液中溶有80 g NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是医生为病人输液时用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签。请认真观察标签上所列内容后填写(该葡萄糖注射液的密度约为1 g·mL-1):

(1)该溶液中含水________g。
(2)该溶液的物质的量浓度约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学按下述操作配制500 mL 0.2 mol·L-1Na2SO4溶液,请回答有关问题。
| 实验步骤 | 有关问题 |
| ①计算所需Na2SO4的质量 | 需要称量Na2SO4的质量为________g |
| ②称量Na2SO4固体 | 称量需要用到的主要仪器是:________________ |
| ③将Na2SO4加入100 mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施?________________________________________________________________________ |
| ④将烧杯中溶液转移至500 mL容量瓶中 | 为了防止溶液溅出,应采取什么措施?________________________________________________________________________ |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1~2 cm处应如何操作?________________________________________________________________________ |
(1)上述实验中使用容量瓶前应_______________________________。
(2)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是________。
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需________。
(4)在实验中,以下操作对实验结果没有影响的是________。
A.没有将洗涤液转移到容量瓶中
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列七种物质:①铝 ②蔗糖 ③CO2 ④H2SO4 ⑤Ba(OH)2
⑥红褐色的氢氧化铁胶体 ⑦HCl
(1)上述物质中属于电解质的有________。(填序号)
(2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是________。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-====H2O,则该反应的化学方程式为____________________________________________。
(4)⑦的浓溶液与高锰酸钾发生反应的化学方程式为:2KMnO4+16HCl(浓)==== 2MnCl2+2KCl+5Cl2↑+8H2O,该反应中的氧化剂是________,盐酸的作用是 ____
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括( )
①原料来源广 ②易燃烧、热值高 ③储存方便 ④制备工艺廉价易行
A ①② B ①③ C③④ D②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com