
一定条件下,体积为1L的密闭容器中存在如下反应:
SiF4(g) + 2H2O(g)  SiO2(s) + 4HF(g) △H= +148.9kJ/mol
SiO2(s) + 4HF(g) △H= +148.9kJ/mol
下列各项中不能说明该反应已达化学平衡状态的是
A.HF体积分数不再变化 B.υ(SiF4) 生成 = 4υ(HF) 生成
C.容器内气体的总质量不再变化 D.生成容器内气体压强不再变化
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源:2017届河北省高三上学期9月月考化学试卷(解析版) 题型:填空题
高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + a Na2O2 = 2Na2FeO4 + b X + 2Na2SO4 + c O2↑
该反应中物质X应是 ,a与c的关系是
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1mol FeO42-转移 mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 mo1。
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三暑假阶段性考试化学试卷(解析版) 题型:填空题
(1)取300 mL 0.2 mol/L的 KI溶液与一定量的酸性 KMnO4 溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量的是________mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 __,又变为棕黄色的原因是用离子方程式解释_________________。
(3)在 100 mLFeBr2 溶液中通入标准状况下2.24 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为________。
(4)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式 _,反应中生成0.2 mol HNO3,转移的电子数目为_______________________。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是_________________。
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三暑假阶段性考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.将100 mL 0.1 mol·L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01NA
B.Na2O2与足量的水反应生成1 mol O2,转移电子数目为2NA
C.某密闭容器中有2 mol SO2和1 mol O2,在一定条件下充分反应,转移的电子数为4NA
D.18 g重水(D2O)所含的电子数为NA
查看答案和解析>>
科目:高中化学 来源:2017届广西省桂林市高三上第二次月考化学试卷(解析版) 题型:填空题
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。下图是工业上用印刷电路的蚀刻液的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:
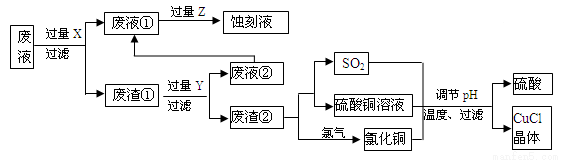
按要求回答下列问题:
⑴ 废液①的主要含有的金属阳离子是__________(填化学符号,下同);废渣①的成分是_____________,Y为__________。
⑵废液①与Z反应的离子方程式为:______________________。
⑶ 写出废渣②生成二氧化硫的化学方程式_____________________。
⑷ 为得到纯净的CuCl晶体,可用下列_________(填序号)进行洗涤。
a.纯净水 b.乙醇 c.稀硫酸 d.氯化铜溶液
⑸ 生产过程中调节溶液的pH不能过大的原因是___________________。
⑹ 写出产生CuCl的离子方程式_______________________。
⑺ 氯化亚铜的定量分析:
① 称取样品0.25g加入10mL过量的FeCl3溶液250mlL锥形瓶中,不断摇动;
② 待样品溶解后,加水50mL和2滴指示剂;
③ 立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点;
④ 重复三次,消耗硫酸铈溶液平均体积为25.00mL。
已知:CuCl的分子式量为99;CuCl + FeCl3 = CuCl2 + FeCl2; Fe2+ + Ce4+ = Fe3+ + Ce3+。
则CuCl的纯度为____________。
查看答案和解析>>
科目:高中化学 来源:2017届广西省桂林市高三上第二次月考化学试卷(解析版) 题型:选择题
下列粒子组在指定介质中一定能大量共存的是
A.酸性溶液中:C2H5OH、Na+、MnO4-、NO3-
B.溶有二氧化硫气体的溶液中:NH4+、Fe2+、SO42-、Cl-
C.加入铝产生H2的溶液:Na+、K+、HCO3-、AlO2-
D.常温下,水电离c(H+)=1×10-10mol·L-1的溶液:Al3+、Cu2+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源:2017届广西省桂林市高三上第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.石灰石、生石灰、熟石灰均属于碱
B.Na2O、MgO、Al2O3均属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上第一次质检化学试卷(解析版) 题型:选择题
已知氨水的密度小于1g/cm3,现将质量分数为15%的氨水与水等体积混合后所得稀氨水的质量分数为
A.7.5% B.大于7.5%. C.小于7.5% D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上9月月考化学卷(解析版) 题型:选择题
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,下列关于X、Y、Z、W 四种元素的描述,不正确的是
A. 原子半径:X>Y>Z>W
B. 原子序数:Y>X>Z>W
C. 原子最外层电子数:Z>W>Y>X
D. 金属性:X>Y,还原性:W2->Z-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com