
下列实验操作正确的是: ( )
编号 | 实验 | 操作 |
A | 实验室用自来水制备蒸馏水 | 将自来水倒入烧杯中,小心给烧杯加热 |
B | 配制一定浓度的氯化钾溶液100mL | 将称好的氯化钾固体放入100 mL容量瓶中,加水溶解,振荡摇匀,定容 |
C | 检验溶液中是否含SO42- | 先加入稀盐酸,无明显现象,再加入BaCl2溶液 |
D | 取出分液漏斗中的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
A. A B. B C. C D. D
科目:高中化学 来源:2016-2017学年江西省南昌市高二上学期期末考试化学试卷(解析版) 题型:简答题
短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B原子的价电子数等于该元素最低化合价的绝对值,C与D能形成D2C和D2C2两种化合物,而D是同周期中金属性最强的元素,E的负一价离子与C和A形成的某种化合物分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为_______________。
(2)已知:①E-E→2E·;△H=+a kJ·mol-1
② 2A·→A-A;△H=-b kJ·mol-1
③E·+A·→A-E;△H=-c kJ·mol-1(“·”表示形成共价键所提供的电子)
写出298K时,A2与E2反应的热化学方程式____________________________________。
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g);△H=-dJ·mol-1(d>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2 molA2、1 molBC | 1 molX | 4 molA2、2 molBC |
平衡时n(X) | 0.5mol | n2 | n3 |
反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
体系的压强 | P1 | P2 | P3 |
反应物的转化率 | α1 | α2 | α3 |
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则该时间段内A2的平均反应速率v(A2)________。
②该温度下此反应的平衡常数K的值为___________。
③三个容器中的反应分别达平衡时各组数据关系正确的是_______(填序号)。
A.α1+α2=1 B.Q1+Q2=d C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0mol F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为65.5%,请在下图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。_______

查看答案和解析>>
科目:高中化学 来源:河北省2016-2017学年高一下学期开学考试化学试卷 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述错误的是
A. 含14g硅原子的二氧化硅晶体中含有的硅氧键数目为2NA
B. 3.9g Na2O2晶体中含有0.2NA个离子
C. 常温常压下,5g D2O含有的质子数、电子数、中子数均为2.5NA
D. 3mol H2和1mol N2在一定条件下反应所得混合气体分子数大于2NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列关于胶体和溶液的说法中,正确的是
A. 分散系的分类: 分散系微粒直径
分散系微粒直径
B. 溶液是电中性的,而胶体是带电的
C. 光线通过时,溶液产生丁达尔效应,胶体则无丁达尔效应
D. 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团农二师华山中学高一下学期学前考试化学试卷(解析版) 题型:推断题
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑
④X+Ca(OH)2―→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是W:________、X:________、Y:________、Z________。
(2)以上4个化学反应,属于氧化还原反应的是______________(填反应序号),反应中氧化剂是__________(写化学式),氧化产物是____________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:
①离子方程式:_____________________________________________。
②化学方程式:________________________________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团农二师华山中学高一下学期学前考试化学试卷(解析版) 题型:选择题
用98%(质量分数)的浓硫酸来配制一定体积的1.0mol·L-1的稀硫酸时,下列仪器不需要用到的是
A. 玻璃棒 B. 胶头滴管 C. 托盘天平 D. 容量瓶
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省广州市高一上学期期期末考试化学试卷(解析版) 题型:实验题
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
【查阅资料】1、无水FeCl3在空气中易潮解,加热易升华。
2、氯气(Cl2)是一种有毒的黄绿色气体,能与NaOH溶液反应。
【实验探究】学习小组设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
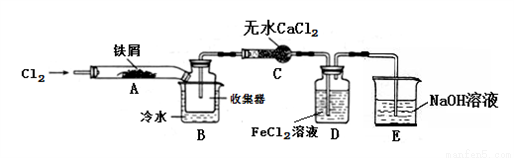
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为:______________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是:____________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填操作步骤序号)____________。
(4)装置D中FeCl2溶液全部反应后,因失去吸收Cl2的作用而失效,写出证明FeCl2溶液已经失效的操作方法:________________。
(5)该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到黄色固体。请写出该反应的离子方程式:__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省广州市高一上学期期期末考试化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。下列物质用途不正确的是
A. Na2O2 是强氧化剂,有漂白性,可用作食品的漂白剂
B. Al2O3熔点很高,可用作耐火材料,制作耐火管和耐火坩埚
C. NaHCO3能与酸反应,可制成胃药治疗胃酸过多
D. Fe2O3是红棕色固体,可用作红色油漆和涂料
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是( )
A. 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH4+
B. 向Na2O2中加入足量的水:2Na2O2+2H2O=4Na++4OH﹣+O2↑
C. 向硫酸铝溶液中加入过量氨水:Al3++3OH﹣=Al(OH)3↓
D. 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3﹣+2OH﹣=CaCO3↓+CO32﹣+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com