
 BaS+4CO↑
BaS+4CO↑ H2SO4+HCl
H2SO4+HCl Na2SO4+NaCl
Na2SO4+NaCl 3S↓+3H2O
3S↓+3H2O CuS↓+H2SO4
CuS↓+H2SO4 Na2S+2H2O
Na2S+2H2O

科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④⑤ | B.②④⑤⑥ |
| C.②③④⑤ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 溶液+气体;
溶液+气体; 溶液+沉淀;
溶液+沉淀; 溶液+沉淀X;
溶液+沉淀X; 溶液Y+沉淀;
溶液Y+沉淀; Y溶液+气体。
Y溶液+气体。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
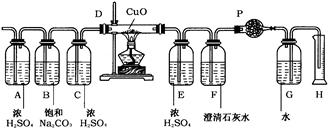
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓H2SO4、稀H2SO4都难挥发 |
| B.浓H2SO4、稀H2SO4都有氧化性,故浓、稀H2SO4都是氧化性酸 |
| C.浓H2SO4、稀H2SO4在加热时都能与铜反应 |
| D.浓H2SO4、稀H2SO4在常温下都能用铁制容器储存 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓硫酸具有强氧化性,稀硫酸无氧化性。 |
| B.稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌。 |
| C.浓硫酸不慎沾到皮肤上,应立即用布拭去,再用水冲洗。 |
| D.浓硫酸与铜的反应中,浓硫酸只表现强氧化性。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com