
分析 (1)将已知方程式变型得到目标方程式,依据盖斯定律计算反应热;升高温度、增大压强、加入催化剂、增大浓度、增大接触面积等措施可以加快反应速率;
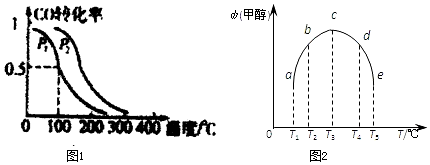
(2)①由图1可知,温度相同时,在压强为P2时平衡时CO的转化率高,由反应CO(g)+2H2(g)?CH3OH(g)可知压强越大,越有利于平衡向正反应进行;
②由图1可知,在P1压强下,100℃时,CO的转化率为0.5,据此计算CO的浓度变化量,根据三段式计算平衡时各组分的平衡浓度,计算合成甲醇的化学平衡常数;
③在其它条件不变的情况下,向容器中通入CO、H2、CH3OH各0.5amol,等效减小氢气的浓度,平衡向逆反应移动;
④在其它条件不变的情况下,再增加a mol CO和2a molH2,相当于压强增大,平衡正向进行达到新平衡时;
(3)根据影响化学反应速率和化学平衡的因素进行判断得出正确结论.a、b没有达到平衡状态,c、d、e达到平衡状态.
解答 解:(1)①CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-764.5kJ•mol-1
②CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1,
依据盖斯定律②+③×2-①得:CO(g)+2H2(g)═CH3OH(g)△H,则△H=△H2+2△H3-△H1=-90.1KJ/mol;
反应为气体体积减小的放热反应,能够增大上述合成甲醇反应的反应速率的是,
a.使用高效催化剂,降低反应的活化能,可以加快反应速率,故a正确;
b.降低反应温度减慢反应速率,故b错误;
c.增大体系压强反应速率增大,故c正确;
d.不断将CH3OH从反应混合物中分离出来,生成物难度减小,反应速率减小,故d错误;
故选ac,
故答案为:-90.1; a、c;
(2)①由图1可知,温度相同时,在压强为P2时平衡时CO的转化率高,由反应CO(g)+2H2(g)?CH3OH(g)可知压强越大,
越有利于平衡向正反应进行,故压强P1<P2,
故答案为:小于;
②由于平衡常数与压强没有关系,所以根据图象可知,在100℃P1时,CO的转化率是0.5,则
CO(g)+2H2(g)=CH3OH(g)
起始浓度(mol/L) $\frac{a}{V}$ $\frac{2a}{V}$ 0
转化浓度(mol/L) $\frac{a}{2V}$ $\frac{a}{V}$ $\frac{a}{2V}$
平衡浓度(mol/L) $\frac{a}{2V}$ $\frac{a}{V}$ $\frac{a}{2V}$
所以平衡常数K=$\frac{\frac{a}{2V}}{\frac{a}{2V}×(\frac{a}{V})^{2}}$=$\frac{{V}^{2}}{{a}^{2}}$,
故答案为:$\frac{{V}^{2}}{{a}^{2}}$;
③在其它条件不变的情况下,向容器中通入CO、H2、CH3OH各0.5amol,等效减小氢气的浓度,平衡向逆反应移动,
故答案为:向左;
④在其它条件不变的情况下,再增加a mol CO和2a molH2,相当于压强增大,平衡正向进行达到新平衡时,CO的转化率增大,
故答案为:增大;
(3)反应进行到t时刻时,a、b没有达到平衡状态,c、d、e达到平衡状态,故T1-T2区间,化学反应未达到平衡状态,温度越高,化学反应速率越快,所以甲醇的体积分数随着温度的升高而提高.T3-T4区间,化学反应已达到平衡状态,由于正反应为放热反应,温度升高平衡向逆反应方向移动,所以甲醇的体积分数减少,
故答案为:T1-T2区间,化学反应未达到平衡状态,温度越高,化学反应速率越快,所以甲醇的体积分数随着温度的升高而提高.T3-T4区间,化学反应已达到平衡状态,由于正反应为放热反应,温度升高平衡向逆反应方向移动,所以甲醇的体积分数减少;
点评 本题考查了热化学方程式和盖斯定律的应用、图象分析应用,化学平衡移动原理的分析判断,平衡常数的表示方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥ | B. | ①④⑥⑩ | C. | ①②④⑥ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其他分散系的本质原因是具有丁达尔效应 | |
| B. | 静电除尘除去空气中的飘尘是利用了胶体粒子的带电性 | |
| C. | 从颜色上无法区别FeCl3溶液和Fe(OH)3胶体 | |
| D. | 在江河入海处容易形成沙洲与胶体的聚沉无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,负极反应为:Zn+4OH--2e-=Zn(OH)42- | |
| B. | 充电时,电解质溶液中K+向阳极移动 | |
| C. | 充电时,电解质溶液中c(OH-)逐渐减小 | |
| D. | 放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
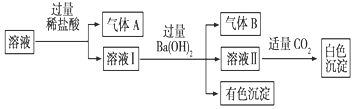 某水溶液中可能存在Na+、Al3+、Fe2+、NH4+、NO3-、CO32-、SO42-中的若干种离子,且存在的各离子具有相同的物质的量,某同学对该溶液进行如图实验,下列判断正确的是( )
某水溶液中可能存在Na+、Al3+、Fe2+、NH4+、NO3-、CO32-、SO42-中的若干种离子,且存在的各离子具有相同的物质的量,某同学对该溶液进行如图实验,下列判断正确的是( )| A. | 气体A一定是CO2,气体B一定是NH3 | |
| B. | 白色沉淀一定是Al(OH)3 | |
| C. | 溶液中一定存在Fe2+、NO3-、NH4+、SO42- | |
| D. | 溶液中可能存在Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
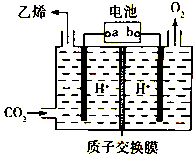 CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题.如图所示电解装置可将CO2转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极.下列有关说法正确的是( )
CO2是重要的温室气体,对地球温室效应的“贡献”最大,如何利用CO2是摆在科技工作者面前的重要课题.如图所示电解装置可将CO2转化为乙烯,该装置的电解质溶液为强酸性水溶液,电极材料为惰性电极.下列有关说法正确的是( )| A. | a为电池的正极 | |
| B. | 电解过程中H+移向阳极 | |
| C. | 反应前后溶液的pH保持不变 | |
| D. | 阴极反应式:2CO2+12H++12e-=C2H4+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com