
 甲、乙两池电极材料都是铁棒与碳棒(如图).请回答下列问题:
甲、乙两池电极材料都是铁棒与碳棒(如图).请回答下列问题:分析 (1)甲池属于原电池,铁易失电子作负极,碳作正极,正极上铜离子得电子发生还原反应;乙池属于电解池,根据电子流向知,C电极为阳极,铁电极为阴极,阴极上铜离子得电子发生还原反应,阳极上氢氧根离子失电子;
(2)①若电解质溶液为氯化钠溶液,则甲中正极上为氧气得电子;
②若电解质溶液为氯化钠溶液,则乙中为电解氯化钠溶液,阳极氯离子失电子,阴极氢离子得电子.
解答 解:(1)甲装置是原电池,铁易失电子作负极,碳作正极,正极上铜离子得电子发生还原反应,生成红色的铜,乙池属于电解池,根据电子流向知,C电极为阳极,铁电极为阴极,阴极上铜离子得电子发生还原反应生成红色的铜,阳极上氢氧根离子失电子生成氧气和水,其电极反应式为:4OH--4e-═2H2O+O2↑;
故答案为:碳;铁;4OH--4e-═2H2O+O2↑;
(2)①若电解质溶液为氯化钠溶液,则甲中正极上为氧气得电子,其电极反应式为:O2+4e-+2H2O═4OH-;
故答案:O2+4e-+2H2O═4OH-;
②若电解质溶液为氯化钠溶液,则乙中为电解氯化钠溶液,阳极氯离子失电子,阴极氢离子得电子,则总反应的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑;
故答案为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
点评 本题综合考查电化学知识,题目侧重于原电池和电解池的原理的考查,注意把握电极反应式的书写,为解答该题的关键,题目难度不大,注意电子的移动方向,为判断电解池的阴极、阳极的关键之处.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
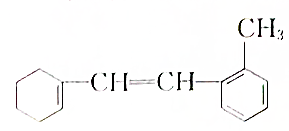 [典型例题√某有机物的结构简式如图:
[典型例题√某有机物的结构简式如图:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Zn+CuSO4 ═ZnSO4+Cu | B. | NaCl+AgNO3═NaNO3+AgCl↓ | ||
| C. | CH3OH+HCOOH→HCOOCH3+H2O | D. | CH4+2Br2 $\stackrel{光照}{→}$ CH2Br2+2HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式: | B. | 石炭酸的结构简式:C6H5OH | ||
| C. | 乙醛的分子式:C2H4O | D. | 酚醛树脂的结构简式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强不再改变 | |
| B. | 气体C在混合气体中所占的物质的量分数不再改变 | |
| C. | 混合气体的密度不再改变 | |
| D. | 单位时间内消耗n mol C的同时消耗2n mol A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 mol•L-1HCl | B. | 4 mol•L-1HNO3 | ||
| C. | 8 mol•L-1NaOH | D. | 18 mol•L-1浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | O | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com