
| A. | Z的分解速率和Y的生成速率相等 | |
| B. | 单位时间内生成nmolZ,同时生成nmolX | |
| C. | 反应体系的总质量保持不变 | |
| D. | X、Y、Z的浓度不再变化 |
分析 当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,据此分析解答.
解答 解:A.Z的分解速率和Y的生成速率相等时,反应方向相同,且其速率之比不等于其计量数之比,所以该反应没有达到平衡状态,故A错误;
B.单位时间内生成nmolZ,同时消耗0.5molnmolX,同时生成nmolX,正逆反应速率不相等,反应没有达到平衡状态,故B错误;
C.无论反应是否达到平衡状态,根据质量守恒定律知,反应前后体系的总质量不变,不能据此判断平衡状态,故C错误;
D.X、Y、Z的浓度不再变化,说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,只有反应前后改变的物理量不变时可逆反应才能达到平衡状态,难点是正确选取平衡状态的判断依据,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 5Cl2+I2+6H2O=10HCl+2HIO3 | B. | MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+H2O | ||
| C. | 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | D. | 2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
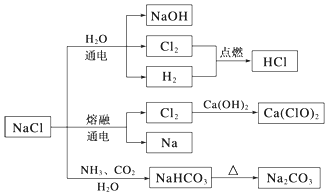
| A. | 由氯化钠制备纯碱的过程中,利用了物质溶解度的差异 | |
| B. | 用Cl2制备漂白粉时,是将Cl2通入澄清石灰水中 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
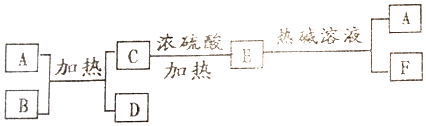
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CO(g)═2C(s)+O2(g) | B. | NH4Cl(s)=NH3(g)+HCl(g) | ||
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g) | D. | MgCO3(s)═MgO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com