
| A. | 0 g | B. | 32 g | C. | 38.4 g | D. | 48 g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol十八烷分子中含有的共价键的数目为54NA | |
| B. | 21g乙烯和丙烯的混合物中所含原子个数为4.5NA | |
| C. | 标准状况下,22.4L的一氯甲烷和二氯甲烷的混合物所含原子的数目为4NA | |
| D. | 1mol/LNa2CO3溶液中,Na+的数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
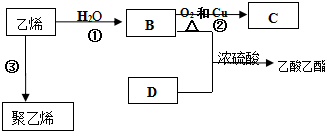
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
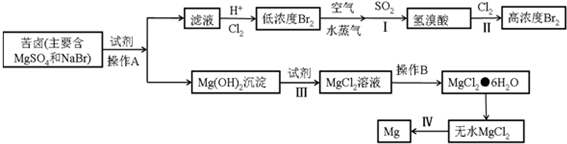
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
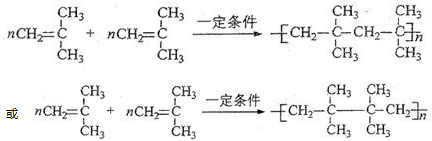 .
.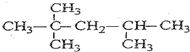 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl原子所含质子数为18,37Cl和35Cl得电子能力相同 | |
| B. | $\frac{1}{18}$mol的H35Cl分子所含中子数约为6.02×1023 | |
| C. | 7 g的35Cl2气体的体积为2.24 L | |
| D. | 35Cl的相对原子质量是12C原子质量的35倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质中至少含有四种元素 | |
| B. | 用饱和的CuSO4溶液使蛋清液发生盐析,进而分离、提纯蛋白质 | |
| C. | 所有的糖类、油脂和蛋白质均能发生水解反应 | |
| D. | 油脂在稀硫酸催化条件下的水解又叫皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO、O2、NO2分子数目比是2:1:2 | |
| B. | 反应混合物中各组分物质的浓度相等 | |
| C. | 混合气体的总质量不变 | |
| D. | 混合气体的平均相对分子质量不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com