
| 序号 | 实验内容 | 实验目的 |
| A | 常温下,测得饱和Na2CO3溶液的pH大于饱和 NaHCO3溶液的pH | 比较常温下水解程度: CO32->HCO3- |
| B | 向2mL甲苯中加入3滴KMnO4酸性溶液,振荡; 向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶 液,前者为黄色,后者为红褐色 | 证明温度升高,Fe3+的水解程度 增大 |
| D | 向盛有10滴0.1mol/LAgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小 的Ag2S沉淀 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Na2CO3溶解度较大,应比较相同的浓度的溶液的pH;
B.甲苯可与酸性高锰酸钾反应;
C.盐类的水解为吸热反应,升高温度促进水解;
D.从难溶电解质的溶解平衡的角度分析.
解答 解:A.饱和溶液的浓度不同,Na2CO3溶解度较大,应比较相同的浓度的溶液的pH,故A错误;
B.甲苯可与酸性高锰酸钾反应生成苯甲酸,而苯不反应,说明与苯环相连的甲基易被氧化,故B正确;
C.盐类的水解为吸热反应,升高温度促进水解,可根据溶液颜色判断,故C正确;
D.再向其中滴加0.1mol/LNa2S溶液,会生成黑色沉淀,说明有Ag2S生成,可说明Ag2S的溶解性更小,故D正确.
故选A.
点评 本题考查化学实验方案的评价,题目难度中等,注意实验的原理和合理性,把握相关物质的性质是解答该题关键.


科目:高中化学 来源: 题型:解答题
 图中A~K分别代表一种物质.已知A易溶于水,分解得到B、C、D的物质的量比为1:1:2,B气体能使品红溶液褪色,C为常见的液体,D气体能使湿润的紫色石蕊试纸变蓝,F为淡黄色固体单质,K为常见的二元强酸,图中有部分生成物未标出.
图中A~K分别代表一种物质.已知A易溶于水,分解得到B、C、D的物质的量比为1:1:2,B气体能使品红溶液褪色,C为常见的液体,D气体能使湿润的紫色石蕊试纸变蓝,F为淡黄色固体单质,K为常见的二元强酸,图中有部分生成物未标出.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 牙膏品牌 | 某儿童牙膏 | 某防臭牙膏 | 某透明牙膏 |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
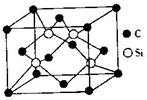 氮化硅是一种重要的结构陶瓷材料,具有优良性能.
氮化硅是一种重要的结构陶瓷材料,具有优良性能.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
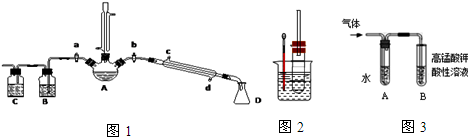
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性KMn04溶液鉴别乙烯和乙炔 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 苯和硝基苯采用分液的方法分离 | |
| D. | 分离沸点相差30℃以上的混溶液体,采用蒸馏的方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com