
(08�Ϻ��ζ�����ĩ)ijʵ��С������ʵ�������Ȼ���ķ��������廯����Ũ����������ͼ��Ϊ��Ҫװ��(�̶������ȵ���������ȥ)��ȡ�廯�����塣

(1) ����װ��������ƿ�е�С�Թܵ�������__________________________________
(2) ʵ�鿪ʼ����������ƿ�в�����������ɫ���塣����ѧ�����ı���Ϊ����ɫ������Ӧ����Ϊ����ɫ��������__________________________���ӱ�ʵ��ķ�Ӧ�������������Ӧ����______________________��
(3) Ϊȷ����������ƿ���ų��������������廯�����壬�����ͼ�ҵ�װ�������飬ָ��ͼ��װ���еĴ���a_________________________��b___________________________��
(4) ͼ��װ�õĹ��ƿ���Թ��зֱ�װ�е��Լ�������( )
A������������Һ����������Һ B�����Ȼ�̼����������Һ
C����������Һ�����Ȼ�̼ D������ˮ����������Һ
(5) ��Ҫ��ʵ������ȡ�⻯�����壬ѡ��ķ�Ӧ����( )
A�������͵� B���⻯�ƺ�Ũ����
C���⻯�غ�Ũ���� D���⻯�غ�Ũ����
��6�����ڼ�װ�õ�������ƿ�зֱ�װ������ҩƷ��aп�ۡ�b�������̷ۡ�c����ʯ�����ֹ���ҩƷ������������ϡ���ᷴӦ����д����ȡ����Ļ�ѧ����ʽ_________________________________________________________________________
 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2(08�㽭ʡ������ѧģ��)ʵ�����и���2SO2��O2![]() 2SO3����H=-393.2 kJ?mol-1�������ͼ��ʾʵ��װ�����Ʊ�SO3���塣��ش��������⡣
2SO3����H=-393.2 kJ?mol-1�������ͼ��ʾʵ��װ�����Ʊ�SO3���塣��ش��������⡣
 |
��1��ʵ��ǰ��������еIJ����ǣ���������ƣ�����д������̣�������������
��2����Aװ���м���Na2SO3�����ͬʱ������Ӽ���ˮ��Ȼ���ٵμ�Ũ���ᡣ�Ӽ���ˮ�������� ��
��3��С�Թ�C��������
��4�����ƿD��ʢ���Լ��� ��װ��D������������ ������ ����
�� ��
��5��ʵ���е�Cr2O3�������ʱ��Ӧ���ƾ����ƿ�һ����ټ��ȣ��Է��¶ȹ��ߣ���������ԭ���� �� ��
��6��װ��F��U�����ռ��������ʵ���ɫ��״̬��
��7��װ��G��������
��8����Gװ�õ�����β������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(08����8У����������)1 Lij�����Һ�����ܺ��е��������±���
���ܴ������е������� |
|
���ܴ������е������� |
|
 ��1��������Һ����μ���
��1��������Һ����μ���![]() ��Һ���ʵ�
��Һ���ʵ�
���ȣ�������������������ʵ�����![]() ��
��
�����![]() ��Һ�������V���Ĺ�ϵ
��Һ�������V���Ĺ�ϵ
����ͼ��ʾ�������Һ��ȷ�����е�����
��_______________������ȷ���Ƿ���
����������______________��Ҫȷ�����
�ڿɲ�������ʵ����___________���϶������ڵ���������_________________��
��2������⣬����Һ�к��д�����![]() ������1 L�û����Һ��ͨ��D���ε�
������1 L�û����Һ��ͨ��D���ε�![]() ����Һ��
����Һ��![]() �����ʵ�����ͨ��
�����ʵ�����ͨ��![]() ���������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺
���������״�����Ĺ�ϵ���±���ʾ��������ش��������⣺

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 (08������Ϣ��)2008�걱�����˻����֡����İ��ˡ���һ����Ҫ�ٴ��Ǽ�������˶�Ա�����˷ܼ�����������һ�ֱ���ֹʹ�õ�ҩ���ṹ��ʽ��ͼ��ʾ�������й�������˵����ȷ���ǣ���
(08������Ϣ��)2008�걱�����˻����֡����İ��ˡ���һ����Ҫ�ٴ��Ǽ�������˶�Ա�����˷ܼ�����������һ�ֱ���ֹʹ�õ�ҩ���ṹ��ʽ��ͼ��ʾ�������й�������˵����ȷ���ǣ���
A������������������������ķ���ʽ��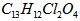
B��1mo1�������������4 mol![]() �����ӳɷ�Ӧ
�����ӳɷ�Ӧ
C������������ڴ���ͬһƽ���ϵ�ԭ����������12��
D������������ ��Һ������ɫ��Ӧ
��Һ������ɫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(08������Ϣ��)һ�����͵��Ҵ���أ�DEFC���û����������ܼ�����200��C����ʱ���磬�Ҵ���رȼ״����Ч�ʸ߳�32���Ҹ���ȫ������ܷ�ӦΪ�� ������˵����ȷ���ǣ���
������˵����ȷ���ǣ���
 A��a��Ϊ��ص�����
A��a��Ϊ��ص�����
B����������ĵ缫��ӦΪ��
C����ع���ʱ������a���ص��߾������ٵ�b��
D����ÿ��������������Ϊq���أ���1mol�Ҵ�����������6 ���صĵ���
���صĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(08����ģ��)�Ϸ�ijԺУ�о����ļ״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
 ��CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H1=+49.0KJ/mol
��CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H1=+49.0KJ/mol
��CH3OH��g��+1/2O2��g��=CO2��g��+2H2��g����H2=-192.9KJ/mol
����˵����ȷ���� ����
A�����ݢ���֪����25�棬101kPaʱ��lmolCH3OH (g��ȼ������
CO2 ��HZO(l���ų�������Ӧ����192.9kJ
B����Ӧ���е������仯����ͼ��ʾ�����H2=E1һE3
C.H2ȼ���ܷų��������ȣ���CH30Hת���H2�Ĺ��̱�����������
D.���ݸ�˹���ɣ������Ƴ�������������Ӧ����1molҺ̬ˮ�ķ�Ӧ�ȡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com