
����Ŀ���١���10��Ԫ����Ԫ�����ڱ��е�λ����ͼ����ش��������⣨�þ���Ԫ�ط��Ż�ѧʽ�Ȼ�ѧ������գ���
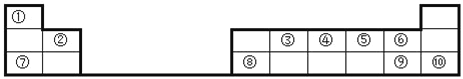
��1��10��Ԫ���л�ѧ�������ȶ�����_____���ǽ�������ǿ����______��
��2������Ԫ�ص�����������Ӧˮ������������ǿ����___________���ѧʽ����
��3���ݢޢߢ���Ӧ�ļ������а뾶��С����________�������ӷ��ű�ʾ����
��4��Ԫ�آܵ�ԭ�ӽṹʾ��ͼ��____________����ҵ���Ԣܵ��⻯��Ϊԭ�Ϻϳɢܵ�����������Ӧˮ����Ļ�ѧ����ʽΪ___________________________��
��5��Ԫ�آ�����������Ӧˮ������Ԫ����������������Ӧˮ���ﷴӦ�����ӷ���ʽ��______________________
���𰸡� Ar F HClO4 Al3+ 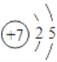 4NH3��5O2
4NH3��5O2![]() 4NO��6H2O��2NO��O2��2NO2��3NO2��H2O��2HNO3��NO Al(OH)3��OH����AlO2����2H2O
4NO��6H2O��2NO��O2��2NO2��3NO2��H2O��2HNO3��NO Al(OH)3��OH����AlO2����2H2O
�����������ݢ١���10��Ԫ����Ԫ�����ڱ��е�λ�ÿ�֪�ֱ���H��Be��C��N��O��F��Na��Al��Cl��Ar����
��1��10��Ԫ���л�ѧ�������ȶ�����ϡ������Ԫ��Ar���ǽ�������ǿ����F����2��Fû�к����ᣬ����Ԫ�ص�����������Ӧˮ������������ǿ����HClO4����3���ݢޢߢ��Ӧ�ļ����ӵĺ�������Ų���ͬ�����Ӱ뾶��ԭ���������������С�������Ӱ뾶��С����Al3+����4����Ԫ�ص�ԭ�ӽṹʾ��ͼ��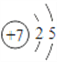 ��������������������NO��NO��������NO2��NO2����ˮ�������ᣬ����ʽ�ֱ���4NH3��5O2
��������������������NO��NO��������NO2��NO2����ˮ�������ᣬ����ʽ�ֱ���4NH3��5O2![]() 4NO��6H2O��2NO��O2��2NO2��3NO2��H2O��2HNO3��NO����5��Ԫ�آ�����������Ӧˮ��������������Ԫ�آ������������Ӧˮ��������������Ӧ�����ӷ���ʽΪAl(OH)3��OH����AlO2����2H2O��
4NO��6H2O��2NO��O2��2NO2��3NO2��H2O��2HNO3��NO����5��Ԫ�آ�����������Ӧˮ��������������Ԫ�آ������������Ӧˮ��������������Ӧ�����ӷ���ʽΪAl(OH)3��OH����AlO2����2H2O��


 �������Ͽ��㱾ϵ�д�
�������Ͽ��㱾ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������˵����ȷ���ǣ� ��
A.0.2molAl������NaOH��Һ��Ӧ�����ɵ�H2������Ϊ0.3NA
B.�����£�1LpH=1��������Һ����ˮ�����H+������ĿΪ0.1NA
C.��״���£�0.1mol�ȷµ����Ϊ2.24L
D.11P4+60CuSO4+96H2O=20Cu3P+24H3SO4+60H2SO4��Ӧ�У�6molCuSO4���������ķ�����Ϊ1.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����о����������ֵĹ����У�ͨ������������Cu��Ni��Zn��Sn��Fe����������
��1��ij�������������ھ��壬������ͷǾ����ͨ���������𣮸ý���������ԭ������ά�ռ�����������������У�����������ԣ�
��2����̬Ni2+�ĺ�������Ų�ʽ�������Ni��CO��4������ΪҺ̬��������CCl4�������л��ܼ�����̬Ni��CO��4 �������壮
��3��ͭ������±�أ�SCN��2��Ӧ����Cu��SCN��2 �� 1mol��SCN��2�����к��ЦҼ�����ĿΪ����±�أ�SCN��2��Ӧ���������֣������������ᣨH��S��C��N���ķе�����������ᣨH��N=C=S���ķе㣬��ԭ������
��4������NiO��������������Ľṹ��ͼ��1��ʾ���侧���߳�Ϊapm����ʽ��ʾNiO������ܶ�Ϊg/cm3�����ؼ��������������ӵ�������ֵΪNA���˹��Ʊ���NiO�����г�����ȱ�ݣ���ͼ��2��һ��Ni2+��ȱ����������Ni2+������Ni3+��ȡ�������������Գʵ����ԣ�����������Ni��O�ı�ֵȴ�����˱仯����֪ij��������Ʒ���Ni0.96O���þ�����Ni3+��Ni2+�����Ӹ���֮��Ϊ �� 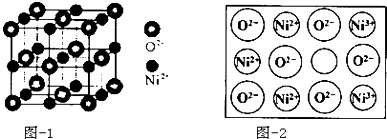
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ش�
��1��H2O2�ĵ���ʽ ��
��2��þȼ�ղ�����CO2����û�ѧ����ʽ��ʾ������ ��
��3���������������ԭ��Ӧ�����ӷ���ʽ��MnO��4+C2O2��4+=Mn2++CO2��+ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1gN2�к���x��ԭ�������ӵ�������
A����x/28��mol-1���� B����x/14��mol-1�� C�� 14x mol-1�� D��28x mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������������ȷ����
A. 62g Na2O����ˮ��������Һ�к���O2-��������ΪNA
B. 50mL 12mol/L��Ũ������������MnO2��ַ�Ӧ��ת�Ƶ�����Ϊ0.3NA
C. 4.4 g D218O��T2O�Ļ����������������Ϊ2.4NA
D. ��״���£�22.4L ������������ˮ��Ӧ��ת�Ƶĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ���G����������ȫ���オ�����ϣ��ڡ���ɫ��Ⱦ���������صĽ���������Ҫ�����ã��й�ת����ϵ���£� 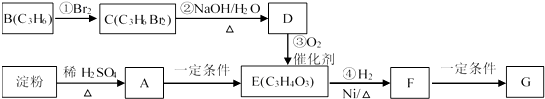
��֪��CH3CH2CH2Br+NaOH��CH3CH2CH2OH+NaBr���������������ˮ�����������ǣ���ش��������⣺
��1������A�ķ���ʽΪ �� B�Ľṹ��ʽΪ��
��2����д��F�к��������ŵ�������
��3����Ӧ�١��������ڼӳɷ�Ӧ������
��4��д����������F�ϳ���Ԫ��������Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ���о�MnO2��˫��ˮ��H2O2���ķ�Ӧ���ʣ�ijѧ������������MnO2��ĩ��50mL�ܶ�Ϊ1.1g/cm3��˫��ˮ��Һ�У�ͨ��ʵ��ⶨ���ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ������ͼ�ش��������⣺ 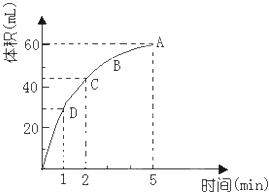
��1���ų�һ����������Ҫ��ʱ��Ϊ��
��2��A��B��C��D���㷴Ӧ���ʿ�����˳���� ��
��3����5min���ռ�������������������ӣ�ԭ���� ��
��4������������Һ�ij�ʼ���ʵ���Ũ��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com