
T℃时。体积均为0.5L的两个恒容密闭容器中发生可逆反应:
2A(g)+B(g) 2C(g)△H=-QkJ/mol(Q>0)
2C(g)△H=-QkJ/mol(Q>0)
实验测得反应在起始、达到平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
A | B | C | ||
① | 2 | 1 | 0 | 0.75Q kJ |
② | 0.4 | 0.2 | 1.6 | |
下列叙述正确的是
A.容器①、②中反应的平衡常数均为36
B.容器②中反应达到平衡时放出的热量为0.05 Q kJ
C.向容器①中通入氦气,平衡时A的转化率不变
D.其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于2/3
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸溶液的浓度和体积 ; ②碱溶液的浓度和体积 ;③比热容;④反应后溶液的质量;⑤ 生成水的物质的量;⑥反应前后温度的变化; ⑦操作所需的时间。
A.①②③⑥ B.③④⑤⑥ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
Mg-AgCl电池是是一种能被海水激活的一次性贮备电池,电池反应方程式:2AgCl+ Mg = Mg2++ 2Ag++2Cl-。有关该电池的说法正确的是
A.Mg为电池的正极
B.负极反应为AgCl+e-=Ag+Cl-
C.不能被KCl溶液激活
D.可用于海上应急照明供电
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是
A.将纯水加热到95℃,KW变大,PH不变,水仍呈中性
B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)降低
C.向水纯中加入少量固体硫酸氢钠,c(H+)增大,KW不变,影响水的电离平衡
D.向水纯中加入醋酸钠或盐酸,均可抑制水的电离,KW不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
在一定温度下的定密闭容器中发生反应H2(g)+I2(g)  2HI(g), 下列说法能说明此反应已经达到平衡状态的是
2HI(g), 下列说法能说明此反应已经达到平衡状态的是
A.容器内每减少1mol I2,同时生产2mol HI
B.容器内气体压强不再变化
C.混合气体的颜色不再变化
D.混合气体的密度恒定不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
pH=1的两种溶液A、B各1mL,分别加水稀释到1000mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图示,下列说法正确的是
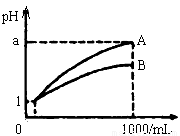
①若a<4,则A、B都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
下图表示可逆反应mA(g)+nB(s) xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是
xC(g)在不同温度和压强下,反应物A的转化率变化情况.下列判断正确的是
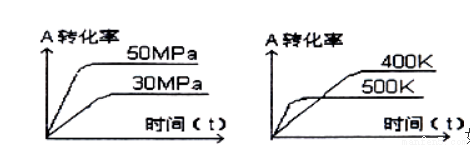
A.m>x,正反应为放热反应
B.m+n<x,正反应为吸热反应
C.m<x,正反应为放热反应
D.m>x,正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江牡丹江高级中学高一上期中化学卷(解析版) 题型:选择题
某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O ,3Cl2+6NaOH=5NaCl+NaClO3+3H2O) ,经测定ClO﹣与ClO3﹣的物质的量之比为1:2,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为
,经测定ClO﹣与ClO3﹣的物质的量之比为1:2,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为
A.21:5 B.11:3 C.3:1 D.4:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨师大附中高一上期中化学卷(解析版) 题型:选择题
下列各组溶液,只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的是
A.HCl和Na2CO3 B.稀H2SO4和NaHCO3
C.CaCl2和Na2CO3  D.Ba(OH)2和NaHSO4
D.Ba(OH)2和NaHSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com