

分析 (1)配制一定物质的量浓度的溶液,需要天平、药匙、玻璃棒、烧杯、量筒、容量瓶和胶头滴管;
(2)因为是用KSCN作指示剂,终点时NH4Fe(SO4)2不再反应,Fe3+与SCN-生成血红色的Fe(SCN)3;
(3)Fe3+与Ti3+反应,生成Fe2+和Ti4+,根据得失电子守恒,有n(Ti3+)×1=n(Fe3+)×1,故n(Fe3+)=n(Ti3+)=n(TiO2)=cV×10-3mol,据此计算其质量分数;
(4)分析错误操作导致V(标准)的变化,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析.
解答 解:(1)配制一定物质的量浓度的溶液,除天平、药匙、玻璃棒、烧杯、量筒外,还需要容量瓶和胶头滴管,即ac,
故答案为:ac;
(2)Fe3+与Ti3+反应,生成Fe2+和Ti4+,加入KSCN不显红色,当达到滴定终点时,再加入NH4Fe(SO4)2溶液,Fe3+过量,与SCN-生成血红色的Fe(SCN)3;
故答案为:溶液变为红色,且半分钟内溶液颜色不变化;
(3)Fe3+与Ti3+反应,生成Fe2+和Ti4+,根据得失电子守恒,有n(Ti3+)×1=n(Fe3+)×1,故n(Fe3+)=n(Ti3+)=n(TiO2)=cV×10-3mol,其质量分数为$\frac{cV×1{0}^{-3}M}{w}$×100%=$\frac{cVM}{1000W}$×100%;
故答案为:$\frac{cVM}{1000W}$×100%;
(4)若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,溶质减少,导致标准液的浓度减少,造成V(标准)减偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,c(标准)偏高;
故答案为:偏高.
点评 本题考查氧化还原滴定法,明确滴定操作方法、原理及误差分析方法是解题的关键,试题侧重考查学生的分析、理解能力及化学实验、化学计算能力.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 明矾可用于净水 | |
| B. | 氨可用于生产铵盐、纯碱 | |
| C. | 铝热反应可用于冶炼某些金属 | |
| D. | 核磁共振氢谱可用于测量某些有机物的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:实验题
实验室要配制100mL1.0mol·L-1的NaCl溶液,试回答下列各题:
(1)经计算,应该用托盘天平称取NaCl 固体________g 。
(2)若用NaCl固体配制溶液,下列仪器中,不需要用到的是_________。(填序号)
A.锥形瓶
B.200mL容量瓶
C.烧杯
D.胶头滴管
E.药匙
F.托盘天平
(3)下列操作中,容量瓶所不具备的功能有_______(填序号)。
A.配制一定体积准确溶度的标准溶液 B.长期贮存溶液
C.用来加热溶解固体溶质 D.量取任意体积的液体
容量瓶上除有刻度线外还应标有_________、__________、且容量瓶在使用前必须__________。
(4)若实验室需要配制0.5mol/L硫酸溶液450mL,则需要质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为________mL(计算结果保留一位小数)。如果实验室有10mL 、25mL、50mL量筒,应选用_______mL规格的量筒最好。
(5)下列四项错误操作会导致所得溶液浓度偏高的是_______(填序号)。
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接进行定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
mgO2中含n个氧原子,则阿伏加德罗常数的值可表示为
A.2n B.16n/m C.32n/m D.n
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
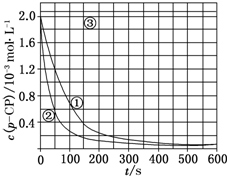 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物.现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响.| 实验编号 | 实验目的 | T/K | pH | c/10-3 mol•L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | 3 | |||
| ③ | 298 | 10 | 6.0 | 0.30 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实 验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | 15 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L甲酸溶液的c(H+)=10-3mol/L | |
| B. | 甲酸以任意比与水互溶 | |
| C. | 10mL 1mol/L甲酸恰好与10mL 1mol/L NaOH溶液完全反应 | |
| D. | 甲酸溶液的导电性比一元强酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ Cu2+ Cl- SO42- | B. | HCO3- NO3- Na+ H+ | ||
| C. | SO42- Cl-Na+ K+ | D. | Na+SO42-H+ AlO2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com