
分析 (1)16kg天然气物质的量近似为$\frac{16g}{16g/mol}$×103=1000mol;
(2)10L水质量近似为10Kg,计算烧开水需要的热量,通常状况下,1molCH4完全燃烧能放出890kJ热量计算得到甲烷的物质的量,由此计算气体标准状况下的体积.
解答 解:(1)16kg天然气物质的量近似为$\frac{16g}{16g/mol}$×103=1000mol,1molCH4完全燃烧能放出890kJ热量,1000mol甲烷完全燃烧放出热量890000KJ,
答:16kg天然气完全燃烧产生的热量是890000KJ;
(2)10L水质量近似为10Kg,使1kg水的温度升高1℃需热量4.18kJ,计算烧开水需要的热量=10×(100-25)×4.18KJ=3135KJ,1molCH4完全燃烧能放出890kJ热量,则甲烷物质的量=$\frac{3135KJ}{890KJ/mol}$=3.52mol,标准状况下体积=3.52mol×22.4L/mol=78.9L,
答:烧开10L水,至少需要消耗甲烷的体积78.9L.
点评 本题考查了好像反应热量变化的计算,注意题干条件的理解应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
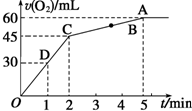 加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g•mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.
加入0.1mol MnO2粉末于50mL过氧化氢溶液(ρ=1.1g•mL-1)中,在标准状况下放出气体的体积和时间的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| CO | H2 | CH3OH |
| 0.5mol•L-1 | 2mol•L-1 | 6mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
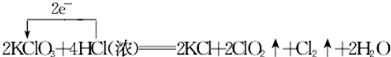 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
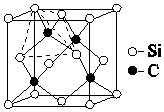 C和Si元素在化学中占有极其重要的地位:
C和Si元素在化学中占有极其重要的地位:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
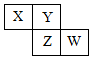 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )| A. | Y单质与氢气反应较Z剧烈 | |
| B. | 最高价氧化物对应水化物酸性W比Z弱 | |
| C. | X单质氧化性强于Y单质 | |
| D. | X与W的原子核外电子数相差9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质的水溶液中不存在分子 | |
| B. | 纯水和干木头都不导电,但木头用水浸湿后却可以导电 | |
| C. | 某溶液的PH=7,该溶液一定呈中性 | |
| D. | 不溶性盐都是弱电解质,可溶性酸和强碱都是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{2}$N2H4(g)+$\frac{1}{2}$O2(g)═$\frac{1}{2}$N2(g)+H2O(g)△H=+267kJ/mol | |
| B. | N2H4(g)+O2(g)═N2(g)+2H2O(l)△H=-534kJ/mol | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=+534kJ/mol | |
| D. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com