

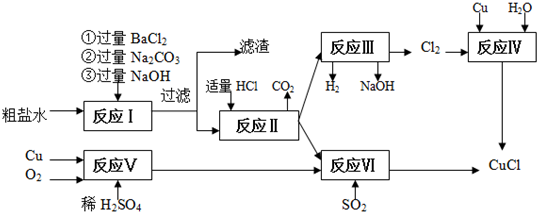
·ÖĪö Ģ¼ĖįøĘ”¢Ģ¼ĖįĆ¾ÓėĻ”ĻõĖį·“Ӧɜ³ÉĻõĻõĖįøĘ”¢ĻõĖįĆ¾Óė¶žŃõ»ÆĢ¼£¬Ģ¼ĖįŃĒĢśÓėĻ”ĻõĖį·“Ӧɜ³ÉĻõĖįĢś”¢¶žŃõ»ÆĢ¼”¢NO£¬ČÜŅŗÖŠ¼ÓČėÅØ°±Ė®£¬Ć¾Ąė×Ó”¢ĢśĄė×Ó×Ŗ»ÆĪŖĒāŃõ»ÆĆ¾”¢ĒāŃõ»ÆĢś³Įµķ£¬¹żĀĖ³żČ„£¬ĀĖŅŗÖŠ¼ÓČėĢ¼Ėįļ§½«ĻõĖįøĘ×Ŗ»ÆĪŖĢ¼ĖįøĘ£¬¹żĀĖ·ÖĄėµĆµ½Ģ¼ĖįøĘ£¬ŌŁÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆøĘ£¬ŌŚ¼ÓČė¹żŃõ»ÆĒā”¢°±ĘųµĆµ½·“Ó¦µĆµ½CaO2£¬ČÜŅŗĄäČ“½į¾§µĆµ½CaO2•8H2O£¬ø±²śĘ·ÖŠŗ¬ÓŠĀČ»Æļ§£®
£Ø1£©·“Ó¦¢ŁÖŠÖ»ÓŠFeCO3ÓėĻõĖį·“Ó¦ŹĒŃõ»Æ»¹Ō·“Ó¦£»
£Ø2£©øĆ·“Ó¦µÄ·“Ó¦ĪļĪŖCaCl2”¢H2O2”¢NH3£¬·“Ӧɜ³ÉCaO2•8H2OÓėNH4Cl£»
H2O2ŹÜČČŅ×·Ö½ā£¬²ÉÓƱłĖ®æŲÖĘĪĀ¶ČŌŚ0”ę×óÓŅ£¬·ĄÖ¹Ęä·Ö½ā£¬ĢįøߥūÓĆĀŹ£¬Ķ¬Ź±ĪĀ¶ČµĶÄܽĻµĶČܽā¶Č£¬Ģįøß²śĀŹ£»
£Ø3£©¹ĢĢåÓÉ2.16g¼ÓČȵ½350”ę±äĪŖ0.56g£¬ŌŚ¼ÓČČ¹ż³ĢÖŠ¹ĢĢåÖŠøĘŌŖĖŲµÄĮæ²»±ä£¬¾Ż“Ė¼ĘĖćŹ£Óą¹ĢĢåÖŠCaŌŖĖŲÖŹĮ棬ĄūÓĆÖŹĮæŹŲŗć¼ĘĖćŹ£Óą¹ĢĢåÖŠOŌŖĖŲÖŹĮ棬½ų¶ųČ·¶Ø»ÆѧŹ½£®
½ā“š ½ā£ŗĢ¼ĖįøĘ”¢Ģ¼ĖįĆ¾ÓėĻ”ĻõĖį·“Ӧɜ³ÉĻõĻõĖįøĘ”¢ĻõĖįĆ¾Óė¶žŃõ»ÆĢ¼£¬Ģ¼ĖįŃĒĢśÓėĻ”ĻõĖį·“Ӧɜ³ÉĻõĖįĢś”¢¶žŃõ»ÆĢ¼”¢NO£¬ČÜŅŗÖŠ¼ÓČėÅØ°±Ė®£¬Ć¾Ąė×Ó”¢ĢśĄė×Ó×Ŗ»ÆĪŖĒāŃõ»ÆĆ¾”¢ĒāŃõ»ÆĢś³Įµķ£¬¹żĀĖ³żČ„£¬ĀĖŅŗÖŠ¼ÓČėĢ¼Ėįļ§½«ĻõĖįøĘ×Ŗ»ÆĪŖĢ¼ĖįøĘ£¬¹żĀĖ·ÖĄėµĆµ½Ģ¼ĖįøĘ£¬ŌŁÓėŃĪĖį·“Ӧɜ³ÉĀČ»ÆøĘ£¬ŌŚ¼ÓČė¹żŃõ»ÆĒā”¢°±ĘųµĆµ½·“Ó¦µĆµ½CaO2£¬ČÜŅŗĄäČ“½į¾§µĆµ½CaO2•8H2O£¬ø±²śĘ·ÖŠŗ¬ÓŠĀČ»Æļ§£®
£Ø1£©·“Ó¦¢ŁÖŠÖ»ÓŠFeCO3ÓėĻõĖį·“Ó¦ŹĒŃõ»Æ»¹Ō·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ3FeCO3+10H++NO3-=3Fe3++NO”ü+3CO2”ü+5H2O£¬
¹Ź“š°øĪŖ£ŗ1£¬3FeCO3+10H++NO3-=3Fe3++NO”ü+3CO2”ü+5H2O£»
£Ø2£©øĆ·“Ó¦µÄ·“Ó¦ĪļĪŖCaCl2”¢H2O2”¢NH3£¬·“Ӧɜ³ÉCaO2•8H2OÓėNH4Cl£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗCaCl2+H2O2+2NH3+8H2O=CaO2•8H2O+2NH4Cl£»
H2O2ŹÜČČŅ×·Ö½ā£¬²ÉÓƱłĖ®æŲÖĘĪĀ¶ČŌŚ0”ę×óÓŅ£¬·ĄÖ¹Ęä·Ö½ā£¬ĢįøߥūÓĆĀŹ£¬Ķ¬Ź±ĪĀ¶ČµĶÄܽĻµĶČܽā¶Č£¬Ģįøß²śĀŹ£¬
¹Ź“š°øĪŖ£ŗCaCl2+H2O2+2NH3+8H2O=CaO2•8H2O+2NH4Cl£»·ĄÖ¹H2O2·Ö½ā£¬ĢįøßĘäĄūÓĆĀŹ»ņ½µµĶCaO2•8H2OČܽā¶Č£¬Ģįøß²śĀŹ£»
£Ø3£©¹ĢĢåÓÉ2.16g¼ÓČȵ½350”ę±äĪŖ0.56g£¬ŌŚ¼ÓČČ¹ż³ĢÖŠ¹ĢĢåÖŠøĘŌŖĖŲµÄĮæ²»±ä£¬Ź£Óą¹ĢĢåÖŠn£ØCa£©=n£ØCaO2•8H2O£©=$\frac{2.16g}{216g/mol}$=0.01mol£¬m£ØCa£©=0.01mol”Į40g/mol=0.4g£¬ŌņŹ£Óą¹ĢĢåÖŠm£ØO£©=0.56g-0.4g=0.16mol£¬¹Źn£ØO£©=$\frac{0.16mol}{16g/mol}$=0.01mol£¬¹Źn£ØCa£©£ŗn£ØO£©=1£ŗ1£¬Ź£Óą¹ĢĢåµÄ»ÆѧŹ½ĪŖCaO£¬
¹Ź“š°øĪŖ£ŗCaO£®
µćĘĄ ±¾Ģāæ¼²é»ÆŹµŃéÖʱø»Æ¹¤Į÷³Ģ”¢·“Ó¦ŌĄķ”¢Ńõ»Æ»¹Ō·“Ó¦µĪ¶ØÓ¦ÓĆ”¢ÓŠ¹ŲĶ¼ĻóµÄ¼ĘĖćµČÓŠ¹ŲĪŹĢā£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õż¶”Ķé | B£® | Ņģ¶”Ķé | C£® | ŅģĪģĶé | D£® | ŠĀĪģĶé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØH+£©=0.1mol/LµÄČÜŅŗ£ŗNa+”¢NH4+”¢SO42-”¢S2O32- | |
| B£® | $\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$=1”Į10-12µÄČÜŅŗ£ŗK+”¢AlO2-”¢CO32-”¢Na+ | |
| C£® | c£ØFe2+£©=0.1mol/LµÄČÜŅŗ£ŗH+”¢Al3+”¢NO3-”¢SCN- | |
| D£® | ŌŚÓÉĖ®µēĄė³öµÄc£ØH+£©=1”Į10-12mol/LµÄČÜŅŗ£ŗFe3+”¢ClO-”¢Na+”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ü | B£® | ¢Ł¢Ū¢Ż | C£® | ¢Ł¢Ś¢Ż | D£® | ¢Ł¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

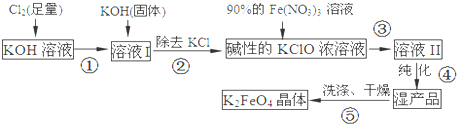
| ŠņŗÅ | ŹµŃé·½°ø | ŹµŃéĻÖĻó | ½įĀŪ |
| ¢Ł | ½«°×É«¹ĢĢåB¼ÓČėĖ®ÖŠ£¬ ¼ÓČČČܽā£¬ĄäČ“½į¾§”¢¹żĀĖ | µĆµ½°×É«¾§ĢåŗĶĪŽÉ«ČÜŅŗ | ĪŽ |
| ¢Ś | ȔɣĮæĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬ µĪČėĻ”HNO3ŗĶAgNO3ČÜŅŗ | Éś³É°×É«³Įµķ | ĀĖŅŗŗ¬Cl- |
| ¢Ū | øÉŌļ°×É«¾§Ģ壬²ā¶ØČŪµć | °×É«¾§ĢåŌŚ122.4”ę×óÓŅĶźČ«ČŪ»Æ | °×É«¾§ĢåŹĒ±½¼×Ėį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | W ÓėY æÉŅŌŠĪ³ÉĄė×Ó»ÆŗĻĪļ | |
| B£® | X µÄ¼ņµ„Ēā»ÆĪļŌŚĶ¬Ö÷×åŌŖĖŲµÄĒā»ÆĪļÖŠ·Šµć×īøߣ¬ĖµĆ÷X µÄ·Ē½šŹōŠŌ×īĒæ | |
| C£® | X ŗĶZ ŠĪ³ÉµÄŌ×ÓøöŹżl£ŗ1 µÄ»ÆŗĻĪļÖŠ£¬¼Čŗ¬ÓŠ¼«ŠŌ¼üÓÖŗ¬ÓŠ·Ē¼«ŠŌ¼ü | |
| D£® | ¹¤ŅµÉś²śÖŠ£¬Ķس£ÓƵē½āZ µÄČŪČŚŃõ»ÆĪļĄ“ÖĘČ”Z µÄµ„ÖŹ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com