
【题目】目前人们正研究开发一种高能电池——钠硫电池,它以熔融的钠、硫为两极,以Na+导电的β″Al2O3陶瓷作固体电解质,反应为2Na+xS![]() Na2Sx。以下说法正确的是( )
Na2Sx。以下说法正确的是( )
A. 放电时,钠作正极,硫作负极
B. 放电时,Na+向负极移动
C. 充电时,钠极与外电源正极相连,硫极与外电源的负极相连
D. 放电时,负极发生的反应是:2Na-2e-===2Na+
【答案】D
【解析】
可充电电池2Na+xS![]() Na2Sx,放电时,作为原电池,Na为负极失去电子,S为正极得到电子。充电时,作为电解池,电极发生的反应与原电池相反,Na为阴极得到电子,S作阳极失去电子。
Na2Sx,放电时,作为原电池,Na为负极失去电子,S为正极得到电子。充电时,作为电解池,电极发生的反应与原电池相反,Na为阴极得到电子,S作阳极失去电子。
A.由分析可知,放电时,Na为负极失去电子,S为正极得到电子,故A错误;
B.放电时,作为原电池,阳离子向正极移动,故Na+向正极移动,故B错误;
C.由分析可知,充电时,作为电解池,电极发生的反应与原电池相反,Na为阴极得到电子,S作阳极失去电子。故钠极与外电源负极相连,硫极与外电源的正极相连,故C错误;
D. 放电时,Na为负极失去电子,负极发生的反应是:2Na-2e-===2Na+,故D正确;
答案选D。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是 ( )
A. 稀硫酸滴在铁片上:2Fe+6H+===2Fe3++3H2↑
B. 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑
C. 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-===Cu(OH)2↓+![]()
D. 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-===AgCl↓+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如下图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如下图乙所示。

请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有______(填字母)。
a.天平 b.烧杯
c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为______________________________________。
(3)AB段反应的离子方程式为______________________________________。
(4)在B点对应的溶液中滴加AgNO3溶液,观察到的现象是________,反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢硫酸是一种二元弱酸,请回答以下问题:
(1)已知 0.1mol/L NaHS 溶液显碱性,则c(S2—)___c(H2S)(填“>”“<”或“=”)。
(2)常温下,向 0.2mol/L的 H2S溶液中逐滴滴入 0.2mol/L NaOH 溶液至中性,此时溶液中以下所示关系不正确的是___(填字母)。
A. c(H+)·c(OH-)=1×10-14
B. c(Na+)=c(HS—)+2c(S2—)
C. c(Na+)> c(HS—)+c(S2—)+ c(H2S)
D. c(H2S)> c(S2—)
(3)已知常温下,CaS 饱和溶液中存在平衡CaS(s) ![]() Ca2+(aq)+S2-(aq) △H>0。
Ca2+(aq)+S2-(aq) △H>0。
①温度升高时,KSP(CaS ) =___ (填“增大”“减少”或“不变”,下同)。
②滴加少量浓盐酸时,c(Ca2+ )___,原因是___(用文字和离子方程式说明)。
③若向CaS 饱和溶液中加入Cu(NO3)2 溶液中,生成一种黑色固体物质,写出该过程中反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3X(g)+Y(g) ![]() W(g)+2M(g) ΔH=-akJ/mol(a﹥0)。一定温度下,在体积恒定的密闭容器中,加入3mol X(g)与1mol Y(g),下列说法正确的是( )
W(g)+2M(g) ΔH=-akJ/mol(a﹥0)。一定温度下,在体积恒定的密闭容器中,加入3mol X(g)与1mol Y(g),下列说法正确的是( )
A. 充分反应后,放出热量为akJ
B. 当反应达到平衡状态时,X与W的物质的量浓度之比一定为3∶1
C. 当X的物质的量分数不再改变,表明该反应已达平衡
D. 若增大Y的浓度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述变化理论上计量结果正确的是( )
A. 标准状况下,用含空气和氨气体积各半的烧瓶进行喷泉实验,所得溶液的物质的量浓度约为![]()
B. 相同质量的两份铝,分别放入足量的![]() 和
和![]() 溶液中充分反应,消耗的
溶液中充分反应,消耗的![]() 和
和![]() 之比为1∶1
之比为1∶1
C. 将![]() 逐滴加入到
逐滴加入到![]() 溶液中,产生
溶液中,产生![]() 的体积约为
的体积约为![]() (标准状况下)
(标准状况下)
D. 向![]() 的
的![]() 溶液中通入足量的
溶液中通入足量的![]() 气体,生成
气体,生成![]() 沉淀
沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验:加热钠至熔化后,停止加热并通入氯气,钠剧烈燃烧并生成大量白烟。以下叙述错误的是
![]()
A.棉花球处发生的离子反应是Cl2+H2O = H++Cl-+HClO
B.大量白烟是氯化钠固体小颗粒
C.钠着火燃烧产生黄色火焰
D.可在棉花球右侧用湿润的淀粉KI试纸判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol MnO2和100 mL 12 mol·L-1盐酸混合后缓缓加热,生成气体单质A,反应完全后向留下的溶液中加入足量AgNO3溶液 (不考虑盐酸的挥发) 。下列说法错误的是
A.在生成气体A的反应中,MnO2是氧化剂,盐酸是还原剂
B.气体单质A是氯气,它的体积是2.24L
C.生成AgCl沉淀的物质的量为1mol
D.整个反应过程被氧化的盐酸有0.4mol,并转移了0.2mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuBr是一种白色晶体,见光或潮湿时受热易分解,在空气中逐渐变为浅绿色。实验室制备CuBr的反应原理为:SO2+2CuSO4+2NaBr+ 2H2O=2CuBr↓+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的的是
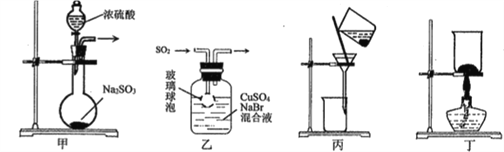
A. 用装置甲制取SO2 B. 用装置乙制取CuBr
C. 用装置丙避光将CuBr与母液分离 D. 用装置丁干燥CuBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com