
| A. | 1-丁烯的键线式: | B. | 乙烯的分子式:CH2=CH2 | ||
| C. | -CHO的电子式: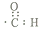 | D. | 丙烷分子的比例模型为: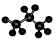 |
分析 A、键线式是用端点或拐点代表碳原子,将H原子省略后所得到的式子;
B、表示物质的元素组成的式子为分子式;
C、-CHO中C原子与O原子形成的是双键,H原子和C原子之间以一对共用电子对结合;
D、用小球和小棍所表示的模型为球棍模型.
解答 解:A、键线式是用端点或拐点代表碳原子,将H原子省略后所得到的式子,而1-丁烯的结构简式为CH3CH2CH=CH2,故键线式为 ,故A正确;
,故A正确;
B、表示物质的元素组成的式子为分子式,乙烯由C原子和H原子组成,且含2个原子和4个H原子,故分子式为C2H4,故B错误;
C、-CHO中C原子与O原子形成的是双键,H原子和C原子之间以一对共用电子对结合,故其正确的电子式为: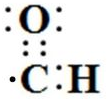 ,故C错误;
,故C错误;
D、用小球和小棍所表示的模型为球棍模型,故 为丙烷的球棍模型,丙烷的比例模型为:
为丙烷的球棍模型,丙烷的比例模型为: ,故D错误.
,故D错误.
故选A.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及球棍模型、分子式、电子式等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生的分析、理解能力及规范答题能力


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火燃烧时用砂子灭火 | |
| B. | 氯水保存在无色透明的试剂瓶中 | |
| C. | 漂白粉保存在烧杯中 | |
| D. | 大量氯气泄漏时用氢氧化钠溶液浸湿的软布蒙面并迅速离开现场 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子晶体中一定存在离子键 | B. | 原子晶体中,只存在共价键 | ||
| C. | 分子晶体的水溶液一定不导电 | D. | 稀有气体能形成分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CO2合成聚碳酸酯可降解塑料,可实现“碳”的循环利用 | |
| B. | 油脂都不能使溴的四氯化碳溶液褪色 | |
| C. | 液化石油气和天然气的主要成分都是烃 | |
| D. | 煤是由有机物和少量无机物组成的复杂混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)氮是地球上含量丰富的一种元素,氮及其化合物在工、农业生产和生活中有着重要作用.
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工、农业生产和生活中有着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: | B. | N2的结构式:N≡N | C. | H2O的球棍模型: | D. | CH4的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随核电荷数的增加 X-的半径递增,还原性递减(用X表示卤素原子) | |
| B. | 氢化物的稳定性随核电荷数的增加逐渐增强 | |
| C. | 单质与水反应均可表示为 X2+H2O═HX+HXO(用X表示卤素原子) | |
| D. | 单质的颜色随核电荷数的增加逐渐加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钙溶液加到醋酸溶液中:Ca(HCO3)2+2CH3COOH═Ca2++2CH3COO-+2CO2↑+2H2O | |
| B. | 漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO3 | |
| C. | Fe-Cu-H2SO4溶液组成的原电池中负极反应式为:Fe-3e-=Fe3+ | |
| D. | 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
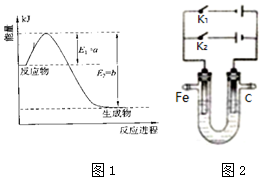
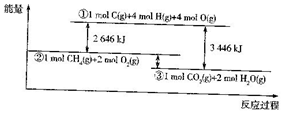 如图表示甲烷和氧气反应过程中的能量变化:请回答下列问题:
如图表示甲烷和氧气反应过程中的能量变化:请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com