
| A. | 聚丙烯的结构简式为: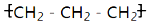 | B. | 硝基苯的结构简式: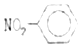 | ||
| C. | 葡萄糖的实验式:CH2O | D. | 甲烷分子的比例模型: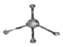 |
分析 A、聚丙烯是丙烯中C=C双键中1个碳碳键断开自身加成反应生成高聚物,链节中主链为2个碳原子;
B、硝基写在苯环的左边时,应该表示为;O2N-;
C、最简式为分子中各原子的最简比;
D、甲烷分子的比例模型应该体现出甲烷分子中各原子的相对体积大小;
解答 解:A、聚丙烯是丙烯中C=C双键中1个碳碳键断开自身加成反应生成高聚物,链节中主链为2个碳原子,聚丙烯的结构简式为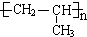 ,故A错误;
,故A错误;
B、硝基写在苯环的左边时,应该表示为;O2N-,硝基苯正确的结构简式为: ,故B错误;
,故B错误;
C、葡萄糖的分子式为:C6H12O6,葡萄糖的实验式为:CH2O,故C正确;
D、甲烷分子的比例模型应该体现出甲烷分子中各原子的相对体积大小, 为甲烷的球棍模型,甲烷的比例模型为:
为甲烷的球棍模型,甲烷的比例模型为: ,故D错误;
,故D错误;
故选C.
点评 本题考查了结构简式、球棍模型与比例模型、实验式等化学用语的判断,题目难度中等,注意掌握常见化学用语的表示方法,明确球棍模型与比例模型的区别.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
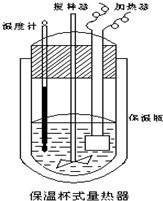 在如图所示的量热计中,将100mL0.50mol•L-1CH3COOH溶液与100mL0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,两溶液的密度均近似为1g•mL-1.下列说法错误的是( )
在如图所示的量热计中,将100mL0.50mol•L-1CH3COOH溶液与100mL0.55mol•L-1NaOH溶液混合,温度从25.0℃升高到27.7℃.已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,两溶液的密度均近似为1g•mL-1.下列说法错误的是( )| A. | CH3COOH溶液与NaOH溶液的反应为吸热反应 | |
| B. | 所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和 | |
| C. | 若量热计的保温瓶绝热效果不好,则所测△H偏大 | |
| D. | CH3COOH的中和热△H为-53.3KJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请填空:
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请填空:查看答案和解析>>
科目:高中化学 来源: 题型:实验题

 CO2+4HCl.
CO2+4HCl.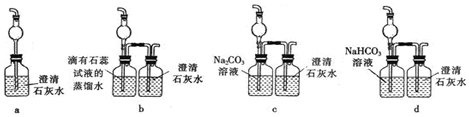
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
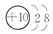 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
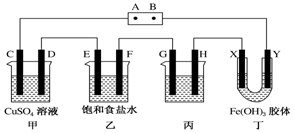
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X只能是第二周期的元素 | B. | a一定比b小 | ||
| C. | b-a+m+n一定等于16 | D. | Y只能是第三周期的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com