
【题目】13C—NMR(核磁共振)可用于含碳化合物的结构分析,表示的碳原子
A. 核外有13个电子,核内有13个质子B. 核内有6个质子,核外有7个电子
C. 质量数为13,原子序数6,核内有7个质子D. 质量数为13,原子序数6,核内有7个中子
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X,Y,Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将153.5g由氯化钠和氯化镁混合而成的盐溶解于水配成1L溶液,测得溶液中Cl—的浓度为3mol/L,则溶液中Na+的物质的量浓度为
A. 2mol/L B. 1 mol/L C. 0.5 mol/L D. 0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2(g)+3H2(g) ![]() 2NH3(g)的能量变化如图所示(△E为能量变化值,a、b、c均为正值)。下列相关说法正确的是
2NH3(g)的能量变化如图所示(△E为能量变化值,a、b、c均为正值)。下列相关说法正确的是

A. 此反应为吸热反应
B. 1mol N+3mol H中的总能量等于1mol NH3中的能量
C. 1mol NH3(l)转变为1mol NH3(g)需要吸收c kJ能量
D. 反应N2(g)+3H2(g) ![]() 2NH3(g)的能量变化值为a+b
2NH3(g)的能量变化值为a+b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晋朝人常璩在《华阳国志》里有这样一段话:临邛县“有火井,夜时光映上昭。民欲其火,先以家火投之。顷许如雷声,火焰出,通耀数十里。以竹筒盛其火藏之,可拽行终日不灭也……”,请回答下列问题。
(1)话中描述的物质是一种最简单有机物甲烷,其分子的结构式为_______。
(2)写出“顷许如雷声,火焰出”涉及的化学反应方程式:_____________________。
(3)下列有关甲烷的说法正确的是________(填选项字母)。
A.它属于化石能源
B.它的分子中含有非极性键
C.它的分子中所有原子的最外层都达到了8电子稳定结构
D.(2)中反应发生时伴随有旧极性键的断裂和新极性键的形成
(4)甲烷不仅可以直接用来燃烧,还是重要的化工原料,它可以与水在高温条件下反应制得水煤气(CO和H2),反应的化学方程式为__________________,反应得到的水煤气中CO和H2的质量比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某溶液中c(Na+)=0.4mol/L,c(Mg2+)=0.25mol/L,c(Cl—)=0.4mol/L,如果溶液中还有SO42—,那么c(SO42—)应为
A. 0.25 mol /LB. 0.15 mol /LC. 0.1 mol /LD. 0.3mol /L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下图所示元素周期表中全部是金属元素的区域为___________
A.A B.B C.C D.D
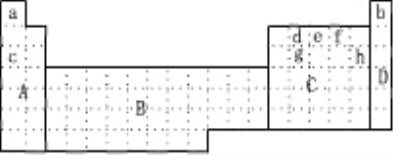
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。______________
②甲、乙两元素相比较,金属性较强的是_________(填名称),可以验证该结论的实验是_______。
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出B的电子式:______,比较C、B、D结合氢离子的能力由强到弱的顺序为_________________(用化学式表示)。
(4)上表中c、h元素形成的简单离子半径之比________ 1(填〉或〈或 =)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com