
有关①100mL 0.1mol/LNaHCO3、②100mL 0.1mol/LNa2CO3两种溶液的叙述不正确的是
A.溶液中水电离出的H+个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO32-)>c(H2CO3)
D.②溶液中:c(HCO3-)>c(H2CO3)
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
已知:25℃时,有关弱酸的电离平衡常数,下列选项中正确的是
弱酸 | H2C2O4 | CH3COOH | HCN | H2CO3 |
电离常数Ki | Ki1=5.9×l0-2 Ki2=6.4×l0-5 | 1.8×l0-5 | 4.9×l0-10 | Ki1=4.3×l0-7 Ki2=5.6×l0-11 |
A.等物质的量浓度的溶液pH关系:NaHCO3>NaCN>CH3COONa>NaHC2O4
B.反应NaHC2O4+NaHCO3→Na2C2O4+H2O+CO2↑能发生
C.等体积等物质的量浓度的溶液中离子总数:NaCN>CH3COONa
D.Na2CO3溶液中2c(Na+)=c(CO32-)+c(HCO3-)+c( H2CO3)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考二化学卷(解析版) 题型:选择题
一小块钠置于空气中,有下列现象:①变成白色粉末;②变暗;③变成白色固体;④变成液体;上述现象出现的先后顺序是
A.①②③④ B.②③④① C.②③①④ D.③②④①
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:填空题
已知:I2+2S2O32-=S4O62-+2I-。相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-29 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2﹒2H2O晶体,加入 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= ;过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2﹒2H2O晶体。
(2)在空气中直接加热CuCl2﹒2H2O晶体得不到纯的无水CuCl2,原因是 。(用化学方程式表示)。由CuCl2﹒2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2﹒2H2O晶体的试样(不含能与I―发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用 作滴定指示荆,滴定终点的现象是 。
②CuCl2溶液与KI反应的离子方程式为 。
③该试样中CuCl2﹒2H2O的质量百分数为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析一定正确的是
A.KSP(PbS)<Kap(CuS)
B.原生铜的硫化物具有还原性,而铜蓝没有还原性
C.CuSO4与ZnS反应的离子方程式是Cu2++S2-═CuS↓
D.整个过程涉及的反应类型有氧化还原反应和复分解反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
常温下,向0.1 mol·L-1的硫酸溶液中逐渐加入物质的量浓度相同的的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验时不同阶段的溶液,下列有关说法中不正确的是

A.溶液的pH:a<b<c<d B.溶液的导电能力:a>b>d>c
C.a、b溶液呈酸性 D.c、d溶液呈碱性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
某可逆反应平衡常数表达式为K=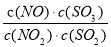 达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
A.反应的热化学方程式为NO2(g)+SO2(g) 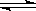 NO(g)(g)+SO3(g) △H>0
NO(g)(g)+SO3(g) △H>0
B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深
C.混合气体的平均摩尔质量保持不变,说明反应已达平衡
D.使用合适的催化剂可使该反应的反应速率和平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上期中理化学卷(解析版) 题型:选择题
实验室用标准盐酸测定某NaOH溶液的浓度,用甲基橙作指示剂,下列对测定结果评价错误的是
选项 | 操作 | 测定结果评价 |
A | 酸式滴定管在装液前未用标准盐酸润洗2~3次 | 偏高 |
B | 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 | 偏高 |
C | 锥形瓶未干燥 | 无影响 |
D | 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 | 偏低 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆兵团二师华山中学高一期中化学卷(解析版) 题型:选择题
下列叙述正确的是
A.1 L水中溶解了40 g NaOH后,所得溶液浓度为1 mol/L
B.从1 L 2 mol/L的NaCl溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.将2.24 L(标准状况)HCl气体溶于水制成100 mL溶液,其物质的量浓度为1 mol/L
D.配制1 L 0.2 mol/L的CuSO4溶液,需用32g胆矾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com