
35 17 |
37 17 |
 与
与  ⑥CH3-CH2-OH和CH3-O-CH3
⑥CH3-CH2-OH和CH3-O-CH335 17 |
37 17 |
 与
与  分子式和结构都相同,是同一物质,
分子式和结构都相同,是同一物质,

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| ||
| A、XZYW | B、ZWXY |
| C、ZXYW | D、ZYXW |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N、O、S |
| B、Cl、N、P |
| C、Be、F、Cl |
| D、F、N、P |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钾跟水反应:K+2H2O=K++2OH-+H2↑ |
| B、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| C、硫酸氢钠溶液与NaOH溶液混合:HSO4-+OH-=H2O+SO42- |
| D、氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用如图所示的装置进行实验:
用如图所示的装置进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:
A、 表示第三周期元素原子半径的变化规律 表示第三周期元素原子半径的变化规律 |
B、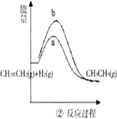 a、b曲线分别表示反应:CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0在使用和未使用催化剂时,反应过程中的能量变化 |
C、 实验用于测定稀盐酸的浓度 |
D、 实验可用于验证HCl在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A、原子半径:rW>rZ>rY>rX |
| B、Y元素的氧化物不能与烧碱溶液反应 |
| C、气态氢化物的热稳定性:Z>W |
| D、X与氢元素组成的化合物XH5与水反应可产生两种气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com