
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中由于哑铃形的C22-存在,使晶胞沿一个方向拉长。下列关于CaC2晶体的说法中正确的是
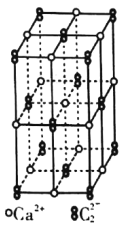
A. CaC2晶体中,所有原子之间都以离子键相结合
B. C22-与N2互为等电子体
C. 1个Ca2+周围距离最近且等距离的C22-数目为6
D. 1个CaC2晶体的晶胞平均含有1个Ca2+和1个C22-
【答案】B
【解析】A. CaC2晶体中含有C22-,C22-原子之间为共价键;B. C22-含电子数为2×6+2=14,N2的电子数为14;C.1个Ca2+周围距离最近且等距离的C22-应位于同一平面,注意使晶胞沿一个方向拉长的特点;D.晶胞中根据均摊法分析微粒的个数.
A. CaC2晶体中,C22-原子之间以供价键相结合,A错误;B.C22-含电子数为:2×6+2=14,N2的电子数为14,二者电子数相同,是等电子体,B正确;C.依据晶胞示意图可以看出,晶胞的一个平面的长与宽不相等,再由图中体心可知1个Ca2+周围距离最近的C22-有4个,而不是6个,C错误;D. 依据晶胞示意图可以看出,1个CaC2晶体的晶胞含有Ca2+为:1+12![]() 和含有C22-为:1+6
和含有C22-为:1+6![]() =4,D错误;答案选B.
=4,D错误;答案选B.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列关于浓硫酸和浓硝酸的叙述中错误的是
A. 加热时两者都能与铜发生反应
B. 两者都具有较强的氧化性
C. 浓硫酸能使蔗糖等有机物炭化,浓硝酸不能
D. 浓硝酸与浓盐酸按质量比为1:3混合可得王水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用一氧化碳和氢气反应生甲醇。一定条件下,在体积为VL的密闭容器中,CO(g)+2H2(g) ![]() CH3OH(g),下图表示该反应在不同温度下的反应过程。关于该反应,下列说法正确的是
CH3OH(g),下图表示该反应在不同温度下的反应过程。关于该反应,下列说法正确的是

A. 反应达平衡后,升高温度,平衡常数K增大
B. 工业生产中温度越低,越有利于甲醇的合成
C. 500℃反应达到平衡时,该反应的反应速率是v(H2)= ![]() mol/(L·min)
mol/(L·min)
D. 300℃反应达到平衡后,若其他条件不变,将容器体积扩大为2VL,c(H2)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列关于溶液中微粒的物质的量浓度关系的描述,不正确的是
A. 0.1mol·L-1HCl溶液与0.2mol·L-1NH3·H2O溶液等体积混合pH>7:c(NH3·H2O)>c(Cl-)> c(NH4+)> c(OH-)
B. pH=8的 NaClO2溶液中:c(Na+)>c(ClO2-)>c(OH-)>c(H+)
C. 向氨水中不断通入CO2,随着CO2的增加,![]() 不断减小
不断减小
D. CH3COOH与NaOH溶液发生中和反应,当醋酸过量时,溶液中可能存在:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH
(1)仅含有共价键的是_________;既有离子键又有共价键的是_________(用序号表示)
(2)离子化合物有_____________________;(用序号表示)
(3)Na2O2 的电子式_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、 B、 C、 D、 E、 F 为前四周期元素且原子序数依次增大,其中基态 A 原子的电子分布在 3 个能级,且每个能级所含的电子数相同; C 的原子核外最外层有 6 个运动状态不同的电子; D 是短周期元素中电负性最小的元素; E 的最高价氧化物的水化物酸性最强; 基态 F 原子核外最外层只有一个电子, 其余能层均充满电子。 G 元素与 D 元素同主族,且相差 3 个周期。
(1)元素 A、 B、 C 的第一电离能由小到大的是____________________(用元素符号表示)。
(2)E的最高价含氧酸中 E 原子的杂化方式为_____________。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为____________________________。
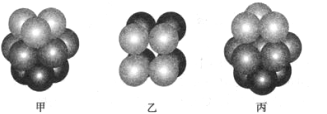
(3)F原子的外围电子排布式为_______________________, F 单质晶体中原子的堆积方式是下图中的_______(填写“甲”、 “乙”或“丙”) ,该晶体的空间利用率为_____________。(保留两位有效数字)
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为__________。
(5)通常情况下, D 单质的熔沸点比 G 单质高,原因是_________________________。
(6)已知 DE 晶体的晶胞如下图所示:
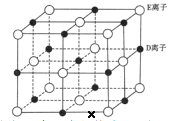
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有_________个 A 原子,该晶体的密度是______________g·cm-3(列式表示) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到固体TiO2。实验室用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为_________________________________。
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________________。
(3)NH4Fe(SO4)2标准溶液盛装在___________(填“酸式”或“碱式”)滴定管中,滴定终点的现象是________________________。若在滴定终点读取滴定管刻度时,仰视标准液液面使测定结果________(填“偏高”“偏低”或“无影响”)。
(4)滴定分析时,称取TiO2(摩尔质量为Mg·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数表达式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用下列几组试剂制取少量NH3:
①固体Ca(OH)2和NH4Cl;②浓氨水和固体CaO;③浓氨水。
请回答下列问题:
(1)用上述三组试剂制取少量NH3,需要加热的是________(填序号),第①组试剂中产生NH3的化学方程式可表示为____________________________________。
(2)下面的制取装置图中,方法①应选用装置________(填“A”或“B”,下同),方法②应选用装置________。
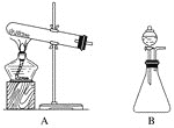
(3)在制取后,如果要干燥氨气,应选用的干燥剂是________(填字母)。
A.浓硫酸 B.固体氢氧化钠 C.五氧化二磷
D.碱石灰 E.固体CaO F.无水CaCl2
(4)检验集气瓶中是否收集满氨气的方法是__________________________________。
(5)为防止环境污染,如下装置(盛放的液体为水)可用于吸收多余NH3的是________(填序号)。
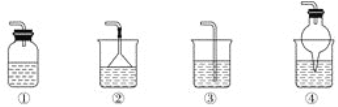
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化)。下列各组物质中,不能满足此转化关系的是( )
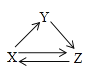
物质 选项 | X | Y | Z |
A | Al | Al2O3 | NaAlO2 |
B | Fe | FeCl3 | FeCl2 |
C | C | CO | CO2 |
D | Cl2 | HCl | NaCl |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com