
����Ŀ����ΪԪ�����ڱ���һ���֣�
̼ | �� | Y | |
X | �� | Z |
���ж� X��Y��Z��������Ӧ��Ԫ�ط��Żش��������⣮
��1��X�� �� ����ԭ��M��������� ��
��2������Ԫ��ԭ�Ӱ뾶������ ��
��3��Y��Ԫ�����ڱ��е�λ���ǵ����ڵ��壬�õ���ʽ��ʾY������⻯����γɹ��� ��
��4�������е�ԭ��֮��Ļ�ѧ�����������ɵ�����������Ӧ����1mol����ʱת�Ƶ��ӵ���Ŀ��NA ��
��5������Z����Ԫ����ȣ��ǽ�����ǿ���� �� ���û�ѧ����ʽ˵����һ���� ��
��6��̼������Y����Ԫ�ص������̬�⻯����ȶ�����ǿ������˳���� �� �����̼Ԫ������ͼ۵�Ԫ����ɻ�����Ļ�ѧʽ�� ��
���𰸡�
��1��Si��4
��2��Si
��3�������� A��![]()
��4�����ۼ���3
��5��Cl��H2S+Cl2=S��+2HCl
��6��H2O��NH3��CH4��C3N4
���������⣺��1�����ݸ�Ԫ�����λ�ÿ�֪��Xλ��̼����һ���壬ΪSiԪ�أ�Si�����M�㺬��4�����ӣ����Դ��ǣ�Si�� 4����2��SiԪ��λ�ڵ������ڣ��ұ��е�������Ԫ����Si��ԭ��������С����Si��ԭ�Ӱ뾶������Դ��ǣ�Si����3��Y��Sλ��ͬһ���壬��YΪOԪ�أ�λ�����ڱ��еڶ����ڢ�A��O���⻯��Ϊˮ��ˮ����Ϊ���ۻ�����õ���ʽ��ʾ���γɹ���Ϊ ![]() �����Դ��ǣ�������A��
�����Դ��ǣ�������A�� ![]() ����4�������е�ԭ��֮��Ļ�ѧ�����ڹ��ۼ�������������NԪ�صĻ��ϼ�Ϊ��3�ۣ����ɵ�����������Ӧ����1mol����ʱת����3mol���ӣ�ת�Ƶ��ӵ���Ŀ��3NA �� ���Դ��ǣ����ۼ���3����5��Z��S��ԭ��������1����ԭ������Ϊ17����ClԪ�أ�Cl��Sλ��ͬһ���ڣ�ԭ������Խ�ǽ�����Խǿ����Cl�ķǽ����Խ�ǿ��ͨ����Ӧ H2S+Cl2=S��+2HCl����֤�������Դ��ǣ�Cl�� H2S+Cl2=S��+2HCl����6���ǽ����ԣ�O��N��C����̼������O����Ԫ�ص������̬�⻯����ȶ�����ǿ������˳���ǣ�H2O��NH3��CH4 �� ̼Ԫ�����̼Ϊ+4��N����ͼ۵�Ϊ��3�������̼Ԫ������ͼ۵�Ԫ����ɻ�����Ļ�ѧʽC3N4 �� ���Դ��ǣ�H2O��NH3��CH4��C3N4 ��
����4�������е�ԭ��֮��Ļ�ѧ�����ڹ��ۼ�������������NԪ�صĻ��ϼ�Ϊ��3�ۣ����ɵ�����������Ӧ����1mol����ʱת����3mol���ӣ�ת�Ƶ��ӵ���Ŀ��3NA �� ���Դ��ǣ����ۼ���3����5��Z��S��ԭ��������1����ԭ������Ϊ17����ClԪ�أ�Cl��Sλ��ͬһ���ڣ�ԭ������Խ�ǽ�����Խǿ����Cl�ķǽ����Խ�ǿ��ͨ����Ӧ H2S+Cl2=S��+2HCl����֤�������Դ��ǣ�Cl�� H2S+Cl2=S��+2HCl����6���ǽ����ԣ�O��N��C����̼������O����Ԫ�ص������̬�⻯����ȶ�����ǿ������˳���ǣ�H2O��NH3��CH4 �� ̼Ԫ�����̼Ϊ+4��N����ͼ۵�Ϊ��3�������̼Ԫ������ͼ۵�Ԫ����ɻ�����Ļ�ѧʽC3N4 �� ���Դ��ǣ�H2O��NH3��CH4��C3N4 ��


 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ���� �� ��
A. 18Oԭ�Ӻ��ڵ�������Ϊ8 B. 16O2��18O2�Ļ�ѧ���ʼ�����ͬ
C. H216O��H218O��������ͬ D. H2��D2 ����ͬλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ�е��ܽ�����ˮ���������治��ȱ�ٵ�������ij����С����õ������ⶨѧУ�ܱߺ�ˮ�е��ܽ�����ʵ�鲽�輰�ⶨԭ�����£�
I.ȡ�������Ĺ̶� .
���ܽ���ƿ�ɼ�ˮ������¼����ѹ��ˮ���¶ȡ���ˮ����Mn(OH)2��������Һ������KI)��ϣ���Ӧ����MnO(OH)2��ʵ�����Ĺ̶���
��.�ữ���ζ�
�ڵ���ƿ�н��������ˮ���ữ��MnO(OH)2��I-��ԭΪMn2+(�÷�Ӧ���ȣ����ڰ�������5min��Ȼ���ñ�Na2S3O3��Һ�ζ����ɵ�I2(2S2O32-+I2=2I- +S4O62-)��
�ش��������⣺
��1�������Ĺ̶����з�����Ӧ�Ļ�ѧ����ʽΪ___________��
��2��ˮ���ữ������Ӧ�����ӷ���ʽ___________��
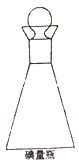
��3���ڵ���ƿ(��ͼ���н��з�Ӧ��Ҫ�����������������ϵ�����ˮ����������Ŀ����___________��
��4��Na2S3O3��Һ���ȶ����ױ�뭻��������ܵ�ˮ��CO2�Լ������Ӱ����ֽ⣬���Ƹ���Һʱ��Ҫ������ˮ���뾭�������ȴ�����ʹ�ã���Ŀ����__________��
��5�� Na2S3O3��Һ���ȶ���ʹ��ǰ��궨��KIO3������궨Na2S3O3��Һ��Ũ�ȣ���ȡ0.214g KIO3�������KI���ã������ĵ���Na2S3O3��Һ�ζ�����ȥ24.00mL����Na2S3O3��Һ��Ũ��Ϊ______����֪M(KIO3) = 214.0g/mol)
��6��ȡ100.00mLˮ�����������ữ���ø�Na2S3O3��Һ�ζ����Ե�����Һ��ָʾ�����յ�����Ϊ_____��������Na2S3O3�����Ϊl0mL����ˮ�����ܽ����ĺ���Ϊ______mg/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�AgCl�ij����ܽ�ƽ��˵������ȷ���ǣ� ��
A.AgCl�������ɺ��ܽⲻ�Ͻ��У��������
B.AgCl������ˮ����Һ��û��Ag����Cl��
C.AgCl����Һ�м���NaCl���壬AgCl�ܽ�Ȳ���
D.���£�AgCl�������ܽ�ȼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������п��ܺ���Cl2��O2��SO2��NO ��NO2�е����ֻ�������塣�ֽ�����ɫ���Ļ������ͨ��Ʒ����Һ��Ʒ����Һ��ɫ����ʣ��������������У��ܿ��Ϊ����ɫ������ԭ�������ɷֵ��ж�����ȷ���ǣ� ��
A���϶���O2��NO B���϶�û��Cl2��O2��NO2
C��������Cl2��O2 D���϶�ֻ��NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�����������������ȷ����( )
A. Al3+���������� B. 2K����2����Ԫ��
C. F2����2����ԭ�� D. 2SO3����3�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж����������ʶ������ȷ����
A. Ũ�����ϡ���ᶼ����������
B. ͭ������ķ�Ӧ�����û���Ӧ
C. Ũ�����ڳ����¼�������Ȼ�ֽ�
D. �����¿�����������ƷʢװŨ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ�Ľ������ϣ���������Ҫ�ɷ���Al2O3��������SiO2��Fe2O3���ʣ��ǹ�ҵ����ȡ����ԭ�ϣ�ʵ����ģ�ҵ����������Ϊԭ����ȡAl2��SO4��3�����������[NH4Al��SO4��212H2O]�Ĺ���������ͼ��ʾ�� 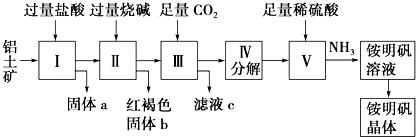 ��ش��������⣺
��ش��������⣺
��1������a�Ļ�ѧʽΪ �� ����ͨ������CO2���巢����Ӧ�����ӷ���ʽΪ ��
��2���ɢ� ��ȡ�������Һ�Ļ�ѧ����ʽΪ �� ���������Һ�л������������ʵ���������Ϊ����������ƣ�����ȴ�ᾧ������ϴ�ӣ�
��3����1000kg��������36%��������Ϊԭ����ȡAl2��SO4��3 �� ��������������98%�����ᣨ�ܶ�1.84gcm��1��L���������뱣��һλС������
��4����ͬʱ��ȡ���������������ͨ����������������������ֲ�Ʒ�IJ���������ʹ�Ƶõ�������������������ʵ���֮��Ϊ1��1����Ͷ��ʱ�������е�Al2O3��H2SO4�����ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������CO2 ͨ��������Һ��:( )
��BaCl2��Һ �ڳ����ʯ��ˮ �۱���Na2CO3��Һ ��K2SiO3��Һ;���ܱ���ǵ���:
A. �٢� B. �٢ڢ� C. �٢ڢۢ� D.�ڢۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com