

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案科目:高中化学 来源:不详 题型:单选题
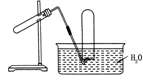
| A.加热NaHCO3制CO2 |
| B.加热NaCl固体与浓硫酸反应制HCl |
| C.用高锰酸钾加热制取O2 |
| D.用Cu与稀硝酸反应制NO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
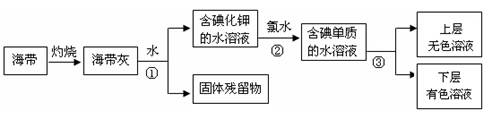

 ( )NaOH+H2↑+( )( )。
( )NaOH+H2↑+( )( )。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
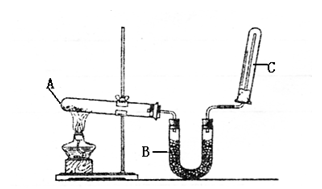
| A.a1=2a2 | B.2a2>a1 | C.a1>2a2 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
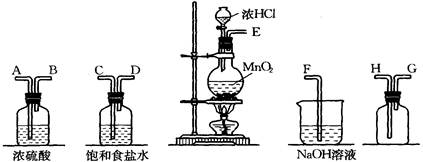
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
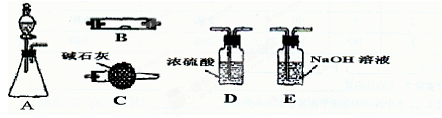
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 %的浓硫酸(ρ= 1.84g/cm3)配制浓度为0.5 mol/L的稀硫酸500mL。有以下几步操作,请按要求回答下列问题:
%的浓硫酸(ρ= 1.84g/cm3)配制浓度为0.5 mol/L的稀硫酸500mL。有以下几步操作,请按要求回答下列问题:  。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com