
【题目】我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂
D.侯德榜联合制碱法
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、 F是周期表中短周期的六种元素,有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 地壳中含量最多的元素 |
B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
E | E与D同周期,且在该周期中原子半径最小 |
F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
(1)请写出B、D、F三种元素的名称: 、 、 。
(2)A与C以原子个数比为1:1形成的化合物的电子式为 ,
将4mol该化合物投入到2L1mol/L BE3溶液中的离子方程式
为 、 。
(3)写出实验室制备F的氢化物的化学方程式 。
(4)下图可用于实验证明D、E的非金属性的强弱。

①溶液a和b分别为 , (写化学式)。
②非金属性D E(填大于或小于),请从原子结构的角度解释原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下非金属氧化物与其引起的环境问题及主要来源对应正确的是 ( )
氧化物 | 环境问题 | 主要来源 | |
A | CO2 | 酸雨 | 化石燃料的燃烧 |
B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
C | NO2 | 温室效应 | 工厂废气的排放 |
D | CO | CO中毒 | 燃料的不完全燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是________________________________________。
(2)装置乙,若电路中转移6.02×1022个e﹣,则C上增加的质量为 。
(3)装置丙中溶液的pH________(填“变大”“变小”或“不变”)。
(4)四种金属活动性由强到弱的顺序是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气在生产、生活和科研中应用十分广泛。
(1)①SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),SNCR-SCR流程中发生的主要反应有:
4NO(g)+4NH3(g)+O2(g) ![]() 4N2(g)+6H2O(g)△H=-1627.2kJmol-1;
4N2(g)+6H2O(g)△H=-1627.2kJmol-1;
6NO(g)+4NH3(g) ![]() 5N2(g)+6H2O(g)△H=-1807.0kJmol-1;
5N2(g)+6H2O(g)△H=-1807.0kJmol-1;
6NO2(g)+8NH3(g) ![]() 7N2(g)+12H2O(g)△H=-2659.9kJmol-1;
7N2(g)+12H2O(g)△H=-2659.9kJmol-1;
反应N2(g)+O2(g) ![]() 2NO(g)的△H= ____________ kJmol-1
2NO(g)的△H= ____________ kJmol-1
②液氨可以发生电离:2NH3(l) ![]() NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式____________;
NH2-+NH4+,COCl2和液氨发生“复分解”反应生成尿素,写出该反应的化学方程式____________;
(2)氨气易液化,便于储运①若在恒温恒容的容器内进行反应2NH3(g) ![]() N2(g)+3H2(g);△H=+94.4kJ/mol,下列表示该反应达到平衡状态的标志有____________(填字母序号)
N2(g)+3H2(g);△H=+94.4kJ/mol,下列表示该反应达到平衡状态的标志有____________(填字母序号)
A.容器中混合气体的密度保持不变
B.NH3(g)百分含量保持不变
C.容器中混合气体的压强保持不变
D.有3个H-H键生成同时又1个N≡N键生成
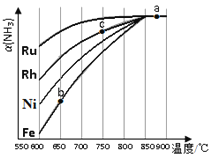
②其他条件相同时,该反应在不同催化剂作用下反应,相同时间后,氨气的转化率随反应温度的变化如图所示.在600℃时催化效果最好的是____________(填催化剂的化学式).c点氨气的转化率高于b点,原因是____________。
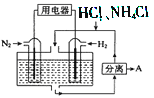
(3)如图表示使用新型电极材料,以N2、H2 为电极反应物,以HCl-NH4Cl为电解质溶液组成的既能提供能量又能实现氮固定的新型电池。请写出该电池的正极反应式____________;生产中可分离出的物质A的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列配合物的配位数不是6的是( )
A.Na3[AlF6]
B.Na2[SiF6]
C.[Cu(NH3)4](OH)2
D.[Pt(NH3)2Cl4]Cl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大。其中基态A原子价电子排布式为nsnnpn+1;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层电子数与B的相同,其余各内层轨道均充满电子。请根据以上信息,回答下列问题(用所对应的元素符号表示):
(1)A、B、E的第一电离能由小到大的顺序为 。
(2)氢化物A2H4分子中A原子采取 杂化。
(3)按原子的外围电子排布分区,元素F在 区,基态F原子的电子排布式为 。
(4)元素A和C可形成一种新型化合物材料,其晶体具有很高的硬度和熔点,其化合物中所含的化学键类型为 。
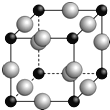
(5)A、F形成某种化合物的晶胞结构如下图所示(其中A显﹣3价,每个球均表示1个原子),则其化学式为 。设阿伏加德罗常数为NA,距离最近的两个F原子的核间距为a cm,则该晶胞的密度为(用含a和NA的代数式表示) g/cm3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com