
| A、SO2(g)+NO2(g)?SO3(g)+NO(g) (正反应为放热反应) |
| B、C(s)+CO2(g)?2CO(g) (正反应为吸热反应) |
| C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g) (正反应为放热反应) |
| D、H2S(g)?H2(g)+S(s) (正反应为吸热反应) |


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
| A、②⑤ | B、①②④ |
| C、②③⑤ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O(g);△H1 2H2(g)+O2(g)=2H2O(l);△H2 | ||
| B、S(s)+O2(g)=SO2(g);△H1 S(g)+O2(g)=SO2(g);△H2 | ||
C、CO(g)+
| ||
| D、NaOH(aq)+HCl (aq)=NaCl(aq)+H2O;△H1 NaOH(aq)+CH3COOH (aq)=CH3COONa (aq)+H2O;△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1个N2分解的同时,有3个H2的形成 |
| B、1个N2分解的同时,有3个H2的分解 |
| C、1个N2分解的同时,有1个NH3的分解 |
| D、1个N2分解的同时,有2个NH3的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽油、柴油和植物油都属于烃 |
| B、乙醇既能被氧化为乙醛也能被氧化为乙酸 |
| C、乙烯和苯加入溴水中,都能观察到褪色现象,原因是都发生了加成反应 |
| D、淀粉和纤维素互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溴苯中混有溴,有汽油箤取出溴 |
| B、硝基苯中混有浓HNO3和浓H2SO4,将其倒入到NaOH溶液中,静置,分液 |
| C、乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 |
| D、乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1溶液中:K+、Mg2+、AlO2-、S2O32- | ||
| B、Na2S溶液中:SO42-、K+、Cl-、Cu2+ | ||
C、
| ||
| D、含Fe2+溶液中:Na+、ClO-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
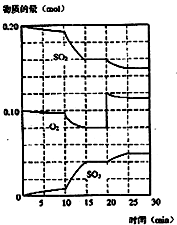 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示| 体系 | c(SO2) mol/L | c(O2) mol/L | c(SO3) mol/L | 反应方向 |
| (1) | 0.0600 | 0.400 | 2.000 | |
| (2) | 0.0960 | 0.300 | 0.500 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com