
| A. | H2S | B. | HNO3 | C. | H2SO4 | D. | H2SO3 |
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,PH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| B. | 1 L 0.1 mol•L-1 Na2SO4溶液中有0.1 NA个Na+ | |
| C. | 一定温度下,1 L 0.50 mol•L-1NH4Cl溶液与2 L0.25mol•L-1NH4Cl溶液含NH4+物质的量不同 | |
| D. | 1L0.1mol•L-1乙酸溶液中H+数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸工业尾气中的SO2用过量的氨水吸收:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| B. | FeO和稀HNO3的反应:FeO+2H+═Fe2++H2O | |
| C. | 向NH4Cl溶液中滴入烧碱溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3•H2O | |
| D. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
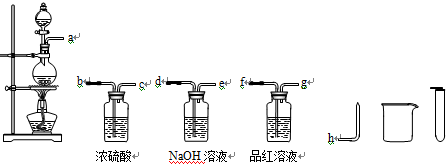
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ④⑥ | C. | ③④⑥ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
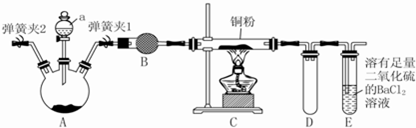
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时OH-向负极移动 | |
| B. | Ag2O2在反应中既是氧化剂又是还原剂 | |
| C. | 每生成1mol Ag外电路转移2 mol电子 | |
| D. | 负极反应为:Zn+4OH--2e-═Zn(OH)42- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com