
 CH3COOC2H5+H2O��
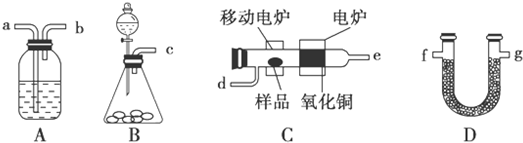
CH3COOC2H5+H2O������ ��1��Bװ���Ʊ���������Cװ���н�����Ʒȼ�գ���ҪAװ���г��Ũ�������������ȼ�պ���Ũ��������ˮ����������Dװ�����ն�����̼������Dװ�����տ�����ˮ�����������̼����ֹӰ�������̼�����ⶨ��
��2��Bװ����ȡO2�����ù�̬ҩƷ��Һ�巴Ӧ�������ǹ���������������̻��߹���������ˮ��Ӧ��
ʵ��ǰ�����ų�װ���еĶ�����̼��ˮ�������Է�������
ֹͣ���Ⱥ�װ���л����һЩȼ�����ɵĶ�����̼��ˮ��������Ҫ�������ų���
��3��Aװ������2.7gΪˮ��������Dװ������4.4gΪ������̼������������C��HԪ�����������������غ㶨���ж��Ƿ�����Ԫ�أ�������ԭ�ӵ����ʵ���֮�����ʵ��ʽ��
��4�����ݣ�3���п���ȷ��X��ʵ��ʽC2H6O��ʵ��ʽ��̼ԭ���Ѿ����ͣ�����X����ʽΪC2H6O��2.3gXΪ0.1mol��X����������Ʒ�Ӧ�ɷų�560mL��������0.25molH2������֪X����ֻ��һ�������ţ�˵��X���Ҵ����Ҵ��������յõ�YΪ���ᣬ�Ҵ������ᷢ��������Ӧ����ZΪ����������
��5��ע�����ʵ����ʵľۼ�״̬�ͷ�Ӧ�ʱ���д�Ȼ�ѧ����ʽ��
��� �⣺��1��Bװ���Ʊ���������Cװ���н�����Ʒȼ�գ���ҪAװ���г��Ũ�������������ȼ�պ���Ũ��������ˮ����������Dװ�����ն�����̼������Dװ�����տ�����ˮ�����������̼����ֹӰ�������̼�����ⶨ��������������ʵ��װ��B��A��C��A��D��D��
�ʴ�Ϊ��A��D��
��2��Bװ����ȡO2�����ù�̬ҩƷ��Һ�巴Ӧ�����õ�ҩƷ��H2O2��MnO2��Na2O2��H2O��
ʵ��ǰ�����ų�װ���еĶ�����̼��ˮ�������Է����������Կ�ʼ��Cװ�ü���֮ǰ��Ҫͨһ��ʱ����������ų�װ���еĶ�����̼��ˮ�����ȣ�
ֹͣ���Ⱥ�װ���л����һЩȼ�����ɵĶ�����̼��ˮ������Ϊȷ��������̼��ˮ���������ų���Ӧ��ͨһ��ʱ���������
�ʴ�Ϊ��H2O2��MnO2��Na2O2��H2O���ų�װ���еĶ�����̼��ˮ�����ȣ���ȼ�����ɵĶ�����̼��ˮ���������ų�������ȫ���գ�
��3��Ũ��������2.7g��ȼ�����ɵ�ˮΪ2.7g����ˮ�����ʵ���Ϊ$\frac{2.7g}{18g/mol}$=0.15mol�����к���Ԫ�ص�����Ϊ0.15mol��2g/mol=0.3g����ʯ������4.4g����ȼ�����ɵ�CO2ˮ4.4g����CO2�����ʵ���Ϊ$\frac{4.4g}{44g/mol}$=0.1mol�����к���̼Ԫ�ص�����Ϊ1.2g����������̼Ԫ�غ���Ԫ�ص�����֮��Ϊ1.2g+0.3g=1.5g��С���л��������2.3g��˵���л�����һ��������Ԫ�أ�����������Ϊ2.3g-1.5g=0.8g����Ԫ�ص����ʵ���Ϊ$\frac{0.8g}{16g/mol}$=0.05mol�����л�����C��H��O����Ԫ�ص����ʵ���֮��Ϊ0.1mol��0.3mol��0.05mol=2��6��1������X���ʵ�ʵ��ʽΪC2H6O��
�ʴ�Ϊ��C2H6O��
��4��X��ʵ��ʽC2H6O��̼ԭ���Ѿ����ͣ����Է���ʽΪC2H6O��2.3gXΪ0.1mol��X����������Ʒ�Ӧ�ɷų�560mL��������0.25molH2������֪X����ֻ��һ�������ţ�˵��X���Ҵ����Ҵ��������յõ�YΪ���ᣬ�Ҵ������ᷢ��������Ӧ����ZΪ����������
�����������Ҵ�����������Ӧ�õ�����������ˮ����Ӧ����ʽΪ��CH3COOH+C2H5OH CH3COOC2H5+H2O��
CH3COOC2H5+H2O��
�ʴ�Ϊ��CH3COOH+C2H5OH CH3COOC2H5+H2O��
CH3COOC2H5+H2O��
����������̼������Һ��Ӧ����������������ˮ����̼������Һ����Ӧ�����ӡ����룬���Գ�ȥ���������л��е�����������Լ��DZ���Na2CO3��Һ���÷�Һ�ķ������룬���������Ƿ�Һ©����
�ʴ�Ϊ������Na2CO3��Һ����Һ©����
��5��2.3g�Ҵ������ʵ���Ϊ$\frac{2.3g}{46g/mol}$=0.05mol������������ȫȼ�����ɶ�����̼�����Һ̬ˮʱ�ɷų�68.35kJ��������1mol�Ҵ���ȫ��Ӧ����68.35kJ��$\frac{1mol}{0.05mol}$=1367kJ���Ȼ�ѧ����ʽΪ��C2H5OH��l��+3O2��g��=2CO2��g��+3H2O��l����H=-1367kJ/mol��
�ʴ�Ϊ��C2H5OH��l��+3O2��g��=2CO2��g��+3H2O��l����H=-1367kJ/mol��
���� ���⿼�����л���������ȷ��ʵ�顢�л���ķ����ᴿ���Ȼ�ѧ����ʽ��д�ȣ��ؼ��Ƕ�ԭ�������⣬�����л������ʽȷ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮú�� | B�� | ��¯ú�� | C�� | ʯ��Һ���� | D�� | ��¯ú�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
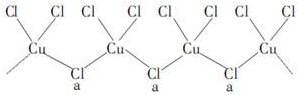
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16O2��18O2��Ϊͬ���칹�� | |
| B�� | 16O��18O��������Ų���ʽ��ͬ | |
| C�� | 16O��18O����������ͬ | |
| D�� | ��״���£�1.12 L 16O2��1.12 L 18O2����0.1 NA ����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
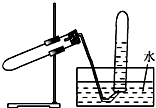 ��ͼ��ʾװ�ÿ����ڣ�������
��ͼ��ʾװ�ÿ����ڣ�������| A�� | ����NaHCO3��CO2 | B�� | ��Cu��ŨHNO3��Ӧ��NO2 | ||
| C�� | ��Zn��ϡ���ᷴӦ��H2 | D�� | ��NaCl��ŨH2SO4������HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ͷ��ˮ�У�Na+2H2O�TNa++2OH-+H2�� | |
| B�� | ���ҽ���Һ�м������ᡢ˫��ˮ��2I-+2H++H2O2�TI2+2H2O | |
| C�� | ̼��������ϡ���ᷴӦ��CO32-+2H+�TH2O+CO2�� | |
| D�� | ��NaAlO2��Һ��ͨ�����CO2��2AlO2-+CO2+3H2O�T2Al��OH��3��+CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | Zn�Ǹ�����Cu������ | B�� | ϡ������Һ��H+����Zn�� | ||
| C�� | ������ͭƬͨ����������пƬ | D�� | ��װ���ܽ�����ת��Ϊ��ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4.6 g�Ҵ��к��е�C-H���ĸ���Ϊ0.6NA | |
| B�� | 34 gH2O2�к��е���������ΪNA | |
| C�� | ��״���£�11.2 LCHCl3�к��еķ�����Ϊ0.5NA | |
| D�� | 9.2gNO2��N2O4��������к��е�ԭ������Ϊ0.6NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com