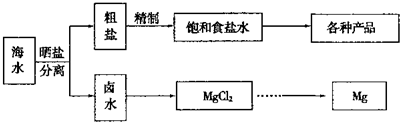
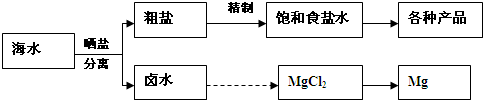
海水中蕴藏着丰富的资源.海水综合利用的流程图如下:
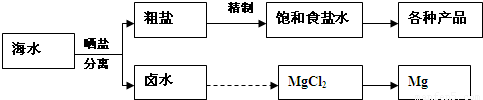
粗盐各种产品卤水MgCl
2Mg晒盐分离海水精制饱和食盐水
(1)用NaCl做原料可以得到多种产品.
①工业上由NaCl制备金属钠的化学方程式是
.
②实验室用惰性电极电解100mL NaCl溶液,若阴阳两极均得到112mL气体(标准状况),则所得溶液的pH为
(忽略反应前后溶液的体积变化).
③电解氯化钠稀溶液可制备“84”消毒液,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式
.
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl
2粗产品.从卤水中提取镁的步骤为:
a.将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
b.将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)
2沉淀;
c.在Mg(OH)
2沉淀中加入盐酸得到MgCl
2溶液,再经蒸发结晶得到MgCl
2?6H
2O;
d.将MgCl
2?6H
2O在一定条件下加热得到无水MgCl
2;
e.电解熔融的氯化镁可得到Mg.
①步骤d中的“一定条件”指的是
,目的是
.
②上述提取镁的流程中,为了降低成本,减少污染,可以采取很多措施,请写出其中一点
.
③有同学认为:步骤b后可加热Mg(OH)
2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则.你同意该同学的想法吗?
,请说出你同意或不同意的理由
.


 2Na+Cl2↑;
2Na+Cl2↑; =0.005mol;
=0.005mol; Cl2↑+H2↑+2NaOH 可知,Cl2↑~H2↑~2NaOH,则n(NaOH)=2n(Cl2)=2×0.005mol=0.01mol,c(NaOH)=
Cl2↑+H2↑+2NaOH 可知,Cl2↑~H2↑~2NaOH,则n(NaOH)=2n(Cl2)=2×0.005mol=0.01mol,c(NaOH)=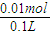 =0.1mol/L,所以pH=13;
=0.1mol/L,所以pH=13; NaClO+H2↑
NaClO+H2↑ 2Na+Cl2↑; 12;NaCl+H2O
2Na+Cl2↑; 12;NaCl+H2O NaClO+H2↑
NaClO+H2↑