
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$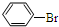 +HBr;
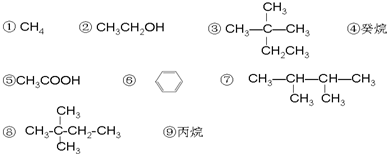
+HBr;分析 (1)结合烷烃的通式CnH2n+2来计算;
(2)由烷烃的通式CnH2n+2,则2n+2=14;
(3)分子式相同,结构不同的有机物互为同分异构体;
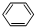
(4)苯与液溴发生取代反应生成溴苯;
(5)碳原子个数越多,沸点越大,相同碳原子个数的烷烃中支链多的沸点低;
(6)乙醇与CuO反应生成乙醛、Cu和水;
(7)该条件下水为气体,反应前后气体的体积没有发生改变,则前后气体的化学计量数相等,根据烃足量的氧气中充分燃烧的通式计算;
(8)乙酸与乙醇发生酯化反应生成乙酸乙酯和水.
解答 解:(1)烷烃的通式为:CnH2n+2,相对分子质量为44的烷烃,则12n+2n+2=44,所以n=3,即烷烃的分子式为C3H8,结构简式为CH3CH2CH3,
故答案为:CH3CH2CH3;
(2)由烷烃的通式CnH2n+2,则2n+2=14,解的n=6,烷烃为C6H14,故答案为:C6H14;
(3)与③互为同分异构体的是⑦,二者分子式相同,结构不同,故答案为:⑦;
(4)具有特殊气味,常作萃取剂的有机物为苯,在铁作催化剂的条件下与液溴发生一取代反应的化学方程式为 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr,
+HBr,
故答案为: +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr;
+HBr;
(5)碳原子个数越多,沸点越大,相同碳原子个数的烷烃中支链多的沸点低,则沸点为④>③>⑨>①,故答案为:④>③>⑨>①;
(6)乙醇与CuO反应生成乙醛、Cu和水,反应为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O,故答案为:CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O;
(7)在120℃,1.01×105Pa条件下,生成的水为气态,由CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O(g),则 1+(x+$\frac{y}{4}$)=x+$\frac{y}{2}$,解得y=4,即分子式中氢原子数目为4,
为甲烷,它与⑧互为同系物,故答案为:①;同系物;
(8)乙酸与乙醇发生酯化反应生成乙酸乙酯和水,该反应为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24 L CCl4中含氯原子数目为0.4NA | |
| B. | 1 mol羟基(-OH)中含电子的数目为10NA | |
| C. | 1mol苯乙烯( )中含碳碳双键数为4NA )中含碳碳双键数为4NA | |
| D. | 2.8g乙烯和环丙烷的混合气体中含原子总数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | B. | 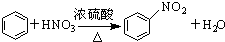 | ||
| C. | 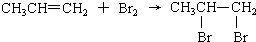 | D. | HCl+AgNO3═AgCl↓?+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④ | C. | ①⑤ | D. | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA个 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol | |
| C. | 17.6 g丙烷中所含的极性共价键为4NA个 | |
| D. | 在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 0.01mol•L-1酸性KMnO4溶液 | 0.1mol•L-1 H2C2O4溶液 | 水 | 反应温度/℃ | 反应时间/s |
| ① | 5.0mL | 5.0mL | 0 | 20 | 125 |
| ② | V1 | V2 | 2.0mL | 20 | 320 |
| ③ | 5.0mL | 5.0mL | 0 | 50 | 30 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com