
| A、NH4+、Mg2+、SO42-、Cl- |
| B、Ba2+、K+、OH-、Cl- |
| C、Al3+、MnO4-、SO42-、Cl- |
| D、Na+、Cu2+、Cl-、Ba2+ |
科目:高中化学 来源: 题型:
| A | NaCl=Na++Cl- NH3?H2O?NH4++OH- | 均属于电离方程式 |
| B | Ba2++SO42-=BaSO4↓ HCO3-+OH-=CO32-+H2O | 均可表示一类反应 |
| C | SO2使酸性高锰酸钾溶液褪色; SO2使碱性酚酞溶液褪色 | 均属于SO2的同一性质 |
| D | Cl2+2NaOH=NaClO+H2O; 3S+6NaOH=2Na2S+Na2SO3+3H2O | Cl2和S在反应中即作氧化剂又作还原剂 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有Fe(NO3)2溶液的试管中加入0.1mol/L H2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| B | 向SO2水溶液中滴入几滴BaCl2溶液,振荡 | 滴加BaCl2后出现白色沉淀 | 此沉淀一定是BaSO3 |
| C | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
| D | 先向2mL 0.1mol/L Na2S溶液中滴入几滴0.1mol/LZnSO4溶液,再加入几滴0.1mol/L CuSO4溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水晶和陶瓷的主要成分都属于硅酸盐 |
| B、单质硅是制造光导纤维的材料 |
| C、硅酸钠是制备硅胶和木材防火剂的原料 |
| D、SiO2是酸性氧化物,它不溶于水也水溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ NO3- Cl- Al3+ |
| B、Mg2+ NH4+ SO42- NO3- |
| C、H+ K+ Cl- CH3COO- |
| D、K+ Al3+ SO42- OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁元素在反应①和③中均被氧化 |
| B、反应②中当有1mol Cl2被还原时,有2mol Br-被氧化 |
| C、氧化性强弱顺序为:Cl2>Br2>Fe3+>I2 |
| D、还原性强弱顺序为:I->Fe2+>Br->Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
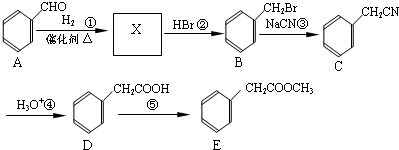
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、植物油可以作为萃取剂分离出碘水中的碘 |
| B、石油的分馏、煤的气化、海水制镁都包括化学变化 |
| C、处理废水时加入明矾作为消毒剂,可以除去水中的杂质 |
| D、乙烯、甲烷、SO2三种无色气体可用溴水鉴别 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com