
分析 (1)赤铁矿的主要成分是氧化铁;
(2)孔雀石的主要成分是碱式碳酸铜;
(3)工业上用电解饱和食盐水的方法制取氯气;
(4)镁在二氧化碳中燃烧生成氧化镁和C;
(5)铜和氯化铁发生氧化还原反应生成氯化亚铁和氯化铜;
(6)碳酸氢钠和氢氧化钠反应的实质是碳酸氢根和氢氧根反应.
解答 解:(1)赤铁矿的主要成分是氧化铁,化学式为Fe2O3,故答案为:Fe2O3;
(2)孔雀石的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3,故答案为:Cu2(OH)2CO3;
(3)电解饱和食盐水生成氢氧化钠和氯气和氢气,离子方程式:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
故答案为:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑;
(4)镁在二氧化碳中燃烧生成氧化镁和C,化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(5)氯化铁和Cu反应生成氯化亚铁和氯化铜,离子反应为Cu+2Fe3+═2Fe2++Cu2+,故答案为:Cu+2Fe3+═2Fe2++Cu2+;
(6)碳酸氢钠溶液和氢氧化钠溶液反应生成碳酸钠和水,离子方程式:HCO3-+OH-=CO32-+H2O;故答案为:HCO3-+OH-=CO32-+H2O;
点评 本题考查化学方程式、离子方程式的书写,掌握物质性质、反应原理和书写方法是解答的关键,题目较简单.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

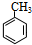 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
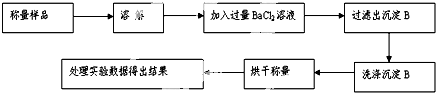
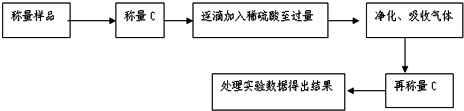

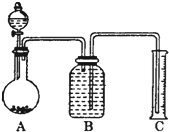
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解 过滤 蒸发结晶 | B. | 加热 溶解 过滤 | ||
| C. | 溶解 过滤 蒸馏 | D. | 溶解 过滤 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
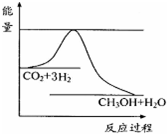 依据事实,写出下列反应的热化学方程式
依据事实,写出下列反应的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:解答题
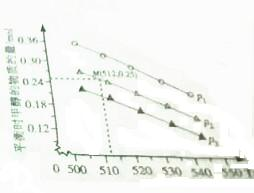 环境问题已经是我国面临的重大问题.
环境问题已经是我国面临的重大问题.| 化学键 | C=O | H-H | C-C | C-H | O-H | C-O |
| 键能/kJ、mol-1 | 803 | 436 | 332 | 409 | 463 | 326 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 系统命名:2,6二甲基辛烷;
系统命名:2,6二甲基辛烷; ;
; ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com