
合成氨反应:3H2+N2 2NH3其反应速率可以分别用v(H2)、v(N2)、v(NH3)[单位均为mol/(L·s)]表示,则正确的关系是
 ( )
( )
A.v(H2)=v(N2)=v(NH3)
B.v(N2)=2v(NH3)
C.v(H2)=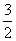 v(NH3)
v(NH3)
D.v(N2)=3v(H2)
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=== NH 4Cl(s)在室温下可自发进行,则该反应的△H<0
4Cl(s)在室温下可自发进行,则该反应的△H<0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH 溶液加水稀释后,溶液中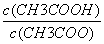 的值减小
的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO.某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验.

已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10﹣5,其饱和溶液中c(OH﹣)约为1×10﹣3mol•L﹣1.请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: .
(2)上述流程中两次使用试剂①,推测试剂①应该是 A (填以下字母编号)
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是 ;(任写一点)
(4)固体E为 ,写出溶液F通入过量CO2生成固体G和溶液H的化学方程式: .
(5)计算溶液F中c(Mg2+)= (25℃时,氢氧化镁的Ksp=5.6×10﹣12)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.合成氨工业中,移走NH3可增大正反应速率,提高原料转化率
B.酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液
C.将NO2、N2O4混合气体的体积压缩为原来的一半,则气体颜色加深
D.牺牲阳极的阴极保护法和外加直流电的阴极保护法都是应用电解原理
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术。反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g)  1/4CaS(s)+CO2(g) ∆H1
1/4CaS(s)+CO2(g) ∆H1
②CaSO4(s)+CO(g)  CaO(s)+CO2(g) +SO2(g) ∆H2
CaO(s)+CO2(g) +SO2(g) ∆H2
③CO(g)  1/2C(s)+1/2CO2(g) ∆H3
1/2C(s)+1/2CO2(g) ∆H3
则反应2CaSO4(s)+7CO(g)  CaS(s)+CaO(s)+6CO2(g)+C(s) +SO2(g)的∆H=
CaS(s)+CaO(s)+6CO2(g)+C(s) +SO2(g)的∆H=
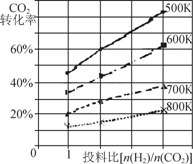 (用∆H1、∆H2和∆H3表示)
(用∆H1、∆H2和∆H3表示)
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH
①该反应平衡常数表达式为K= 。
②已知在某压强下,该反应在不同温度、不同投料
比时,CO2的转化率如右图所示。该反应的ΔH
____(填“>”“<”或“=”)0。若温度不变,减
小反应投料比[n(H2) /n(CO2)],则K将 (填“增大”“减小”或“不变”)。
③二甲醚燃料电池具有启动快,效率高等优点,若电解质为酸性,二甲醚燃料电池的负极反应为 。
(3)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2nCu+(n+1)O2+(2-2n) H2O=2nCuSO4+(2-2n) H2SO4
 从环境保护的角度看,催化脱硫的意义为
从环境保护的角度看,催化脱硫的意义为
。
②利用右图所示电化学装置吸收另一部分SO2,
并完成Cu的再生。写出装置内所发生反应的
总的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下测得某无色溶液中水电离出c(H+)=1×10-11mol/L,又知该溶液中还有大量NO3-、NH4+、Cl-,那么该溶液中还一定大量存在的离子是( )
A.[Al(OH)4]-、ClO- B.Mg2+、SO42-
C.Cu2+、HCO3- D.Ba2+、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
在C(s)+CO2(g)2CO(g)反应中,可使反应速率增大的措施是 ( )
①增 大压强 ②增加炭的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥通入CO
大压强 ②增加炭的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥通入CO
A.①③④ B.②④⑥ C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2===CaCO3↓+H2O
B.碳酸钠溶液中加入二氧化硅:CO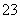 +SiO2===SiO
+SiO2===SiO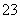 +CO2↑
+CO2↑
C.二氧化硅与烧碱溶液反应:SiO2+2OH-===SiO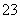 +H2O
+H2O
D.硅酸和烧碱溶液中和:H++OH-===H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
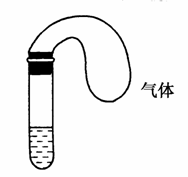
已知NH3溶于水得氨水,呈碱性。某学校课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是
________________________________________________________________________。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是________________________溶液;加热时溶液由无色变为红色的原因是______________________ __________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com