
 人体内的铁是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.
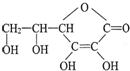
人体内的铁是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.分析 由结构简式可知分子式,含-OH、-COOC-、C=C,结合酯及烯烃的性质来解答;铁与盐酸反应生成氯化亚铁和氢气.
解答 解:(1)服用维生素C可解除中毒,这说明维生素C将铁离子转化为亚铁离子,则具有还原性;高锰酸钾具有强氧化性,与维生素C发生氧化还原反应,高锰酸钾褪色,
故答案为:还原;酸性KMnO4溶液褪色;
(2)由结构简式可知分子式为C6H8O6;由于它能防治坏血病,又称为抗坏血酸,故答案为:C6H8O6;抗坏血酸;
(3)铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐的离子方程式为:Fe+2H+═Fe2++H2↑,
故答案为:Fe+2H+═Fe2++H2↑.
点评 本题考查有机物的结构与性质,为高频考点,侧重于学生的分析能力的考查,注意习题中的信息分析物质的性质,把握官能团与性质的关系为解答的关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该有机物可看作氨基酸,也可看作是酚类物质 | |
| B. | 能与盐酸发生反应 | |
| C. | 能发生取代反应,中和反应,缩聚反应 | |
| D. | 既能与溴水发生取代反应,又能与溴水发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:NH3<PH3<AsH3 | B. | 酸性:H2SO4>H3PO4>H2SiO3 | ||
| C. | 还原性:S 2-<Br -<Fe 2+ | D. | 电负性:Cl>P>S |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2用作呼吸面具的供氧剂 | |
| B. | 工业上电解熔融状态的MgCl2制备Mg | |
| C. | 工业上利用合成氨实现人工固氮 | |
| D. | 实验室用NH4Cl和Ca(OH)2制备NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 | |
| B. | 将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 | |
| C. | 常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) | |
| D. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com