
| A. | 同质量的H2与Cl2,H2的分子数一定比Cl2多 | |
| B. | 0.5mol氢的质量是0.5g | |
| C. | 摩尔是用来衡量微观粒子多少的一种物理量 | |
| D. | 0.1mol H2SO4含有氢原子数的精确值为1.204×1023 |
分析 A.根据n=$\frac{m}{M}$计算二者的物质的量关系,再根据N=nNA计算;
B、0.5mol氢指代不明确;
C、摩尔是物理量的单位;
D、0.1mol H2SO4含有氢原子数是0.2NA.
解答 解:A.H2的摩尔质量为2g/mol,Cl2的摩尔质量为71g/mol,二者质量相同,二者物质的量比为$\frac{m}{2}$:$\frac{m}{71}$=71:2,N=nNA,同质量的H2与Cl2含有的分子数之比为:71:2,H2的分子数一定比Cl2多,故A正确;
B、0.5mol氢指代不明确,故B错误;
C、摩尔是物理量物质的量的单位,故C错误;
D、0.1mol H2SO4含有氢原子数近似为:1.204×1023,不是精确值,故D错误.
故选A.
点评 本题考查学生物质的量以及阿伏伽德罗常数的有关计算知识,注意知识的迁移应用是关键,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
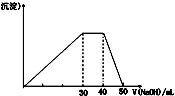 学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:
学习化学要准确掌握化学基本概念和研究方法.按要求回答下列问题:| | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| 第一组 | Na2CO3 | H2SO4 | NaHCO3 | CaO | CO2 |
| 第二组 | NaOH | HCl | NaCl | Na2O | SO2 |
| 第三组 | NaOH | CH3COOH | CaF2 | Al2O3 | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A配置0.10mol/LNaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中的I2分出水层后的操作 | D.记录滴定终点读数为12.20mL |
 |  |  |  |
| A. | 配制0.10mol/L NaOH溶液 | |
| B. | 除去CO中的CO2 | |
| C. | 苯萃取碘水中的I2分出水层后的操作 | |
| D. | 记录滴定终点读数为12.20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如图所示:回答下列问题:
乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如图所示:回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.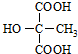 (或
(或 ).
).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始物质的量/mol | 0.1 | 0.3 | 0 |
| 平衡物质的量/mol | 0.05 | 0.2 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+2Y?2Z | |
| C. | 若起始时X、Y、Z的物质的量分别为0.1 mol、0.4mol、0.2mol,达平衡时,Z的体积分数一定增大 | |
| D. | 若起始时X、Y、Z的物质的量分别为0.05 mol、0.15mol、0.1mol,达平衡时,X的转化率一定与原投料相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com