
分析 过量的AgNO3,用0.1021mol•L-1NH4SCN标准溶液返滴,发生反应Ag++SCN-=AgSCN,所以过量的银的物质的量为:n(Ag+)=n(NH4SCN)=8.92m1×0.1021mol•L-1×10-3L/ml=9.1×10-4mol,所以与溴化钾反应的硝酸银的物质的量为:0.1062mol.L-1×30×10-3mol-9.1×10-4mol=2.386×10-3mol,所以25.00m1中含有溴化钾的物质的量为:2.386×10-3mol,则m(KBr)=2.386×10-3mol×119g/mol=0.272g,由此分析解答.
解答 解:过量的AgNO3,用0.1021mol•L-1NH4SCN标准溶液返滴,发生反应Ag++SCN-=AgSCN,所以过量的银的物质的量为:n(Ag+)=n(NH4SCN)=8.92m1×0.1021mol•L-1×10-3L/ml=9.1×10-4mol,所以与溴化钾反应的硝酸银的物质的量为:0.1062mol.L-1×30×10-3mol-9.1×10-4mol=2.386×10-3mol,所以25.00m1中含有溴化钾的物质的量为:2.386×10-3mol,则m(KBr)=2.386×10-3mol×119g/mol=0.272g,试样中KBr的百分含量$\frac{0.272g}{4.1683g×\frac{25.00m1}{250m1}}$×100%=65.25%,答:KBr的百分含量为:65.25%.
点评 本题考查了有关方程式的计算、滴定原理的应用,题目难度中等,侧重于考查学生的分析能力和计算能力,注意把握滴定时溶液中发生的反应.


科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | Zn(OH)2 | C. | MnO2 | D. | MnOOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=一124.2kJ•mol-1 | B. | △H=+124.2kJ•mol-1 | ||
| C. | △H=+248.4kJ•mol-1 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
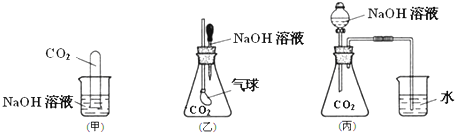
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,有白色沉淀产生,说明蛋白质发生变性 | |
| B. | 苯中含有少量的苯酚可先加适量的浓溴水,使之生成2,4,6三溴苯酚,再过滤除去 | |
| C. | 用溴水检验CH2═CH-CHO中是否含有碳碳双键 | |
| D. | 麦芽糖及其水解产物均能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
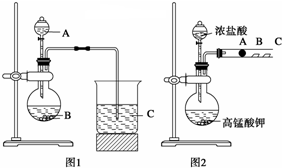
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 为防止催化剂中毒,炉气在进入接触室之前需要净化 | |
| B. | 为提高SO2的转化率,接触室内反应温度选定在400℃~500℃ | |
| C. | 为防止污染大气,从吸收塔出来的尾气常用稀氨水吸收 | |
| D. | 为提高SO3的吸收效率,用稀硫酸代替水吸收SO3. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HCl<HBr<HI | B. | 原子半径:K<Na<Li | ||
| C. | 熔点:Cl2>Br2>I2 | D. | 氧化性:Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com