
根据下列事实:(1)X+Y2+ = X2++Y;(2)Z+2H2O = Z(OH)2+H2  (3)Z2+氧化性比X2+弱;(4)由Y、W电极组成的原电池,电极反应为:W2++2e- = W,Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序是( )
(3)Z2+氧化性比X2+弱;(4)由Y、W电极组成的原电池,电极反应为:W2++2e- = W,Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序是( )
A、X>Z>Y>W B、Z>W>X>Y C、Z>X>Y>W D、Z>Y>X>W
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
现取有机物A 3.00g与4.48L(标准状况)氧气在密闭容器中燃烧,燃烧后产物只有二氧化碳、—氧化碳和水蒸气(没有反应物剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.60g,碱石灰增重4.40g。回答下列问题:
(1)3.00gA中所含氢原子为 mol、碳原子为 mol。
(2)该有机物的分子式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或对实验事实的叙述正确的是 ( )
①用稀盐酸洗涤盛放过石灰水的试剂瓶
②配制FeCl3溶液时,向溶液中加入少量Fe粉和稀盐酸
③用pH试纸测得氯水的pH为2
④用稀硝酸清洗做过银镜反应实验的试管
⑤浓硝酸保存在棕色细口瓶中
⑥将镁条和铝片用导线连接再插进稀NaOH溶液,铝条上产生气泡
⑦某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+
⑧清洗试管内壁的MnO2用双氧水
A.①④⑤⑦ B.②③④⑦ C.①②⑥⑧ D.①⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为7∶17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
A.金属性:Y>Z B.氢化物的沸点:X>W
C.离子的还原性:X>W D.离子半径:Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
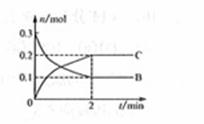
一定温度下,在2L的密闭容器中发生反应:A(g)+2B(g)  xC(g) △H<0,B、C物质的物质的量随时间变化的关系如图。下列说法不正确的是( )
xC(g) △H<0,B、C物质的物质的量随时间变化的关系如图。下列说法不正确的是( )
A. x=2
B. 反应开始2min内,v(C)=0.1mol·L-1·min-1
C. 2min后,降低温度平衡向右移动
D. 当容器内混合气体压强不再改变时,体系达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是( )
A.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
B.2 L0.5 mol • L-1硫酸钾溶液中阴离子所带电荷数为NA
C.1 mol Na2O2固体中含离子总数为4NA
D. 5NH4NO3 2HNO3+4N2↑+9H2O反应中,生成28 gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 gN2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
Ⅰ.Ni(S)+4CO(g)
 Ni(CO)4(g)+Q
Ni(CO)4(g)+Q
Ⅱ.Ni(CO)4(g)  Ni(S)+4CO(g)
Ni(S)+4CO(g)
完成下列填空:
(1)在温度不变的情况下,要提高反应Ⅰ中Ni(CO)4的产率,可采取的措施有_______________________、____________________________。
(2)已知在一定条件下的2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如右图所示。Ni(CO)4在0~10min的平均反应速率为_______________________________。

(3)若反应Ⅱ达到平衡后,保持其他条件不变,降低温度,重新达到平衡时,下列说法正确的是___________。
a.平衡常数K增大 b.CO的浓度减小 c.Ni的质量减小 d.v逆[Ni(CO)4]增大
查看答案和解析>>
科目:高中化学 来源: 题型:
大气中SO2和NOx是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Mg2+、NH 、Cl-、SO
、Cl-、SO 、SO
、SO 、NO
、NO 和NO
和NO 等。某研究小组取该地一定量的酸雨,浓缩后将所得试液分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;第四份加入硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。21教育网
等。某研究小组取该地一定量的酸雨,浓缩后将所得试液分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;第四份加入硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。21教育网
[已知:Ksp(Ag2SO4)=1.20×10-5]
请回答下列问题:
(1)该酸雨中肯定存在的离子有 SO 、NO
、NO 、NH
、NH ;肯定不存在的离子有 SO
;肯定不存在的离子有 SO 、NO
、NO ,说明其不存在的理由:________________________________________________________________________
,说明其不存在的理由:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)写出试液中滴加淀粉KI溶液所发生反应的离子方程式:________________________________________________________________________
________________________________________________________________________。
(3)设计实验方案,检验该试液中是否存在Cl-:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(4)该研究小组为了探究NO参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,慢慢通入O2,该过程中发生的化学反应有________________________________________________________________________、
________________________________________________________________________,
再喷射适量蒸馏水即得硫酸型酸雨。说明NO的作用: 催化剂 。
查看答案和解析>>
科目:高中化学 来源: 题型:
13C-NMR(核磁共振)可用于含碳化合物的结构分析14N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N叙述正确的是( )
A.13C与15N具有相同的中子数 B.13C与C60是同一种物质
C.15N与14N互为同位素 D.15N的核外电子数与中子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com