
| A�� | ���Ӱ뾶��c��b��a | |
| B�� | a��c�γɻ��������Һ�ж���Ҫ�ܷⱣ���ڲ���ƿ�� | |
| C�� | a2b2��d��һ�ֽϸ�̬���ӵ�����Һ���ʱ�����������b2 | |
| D�� | d����������Һ����c�ĵͼ���������������ԭ��Ӧ�����ܴ������� |
���� a��b��c��d��ԭ���������ε���������Ԫ�أ�a��b��c����Ԫ�ص�ԭ�Ӻ��������֮����Cl-�ĺ����������ȣ�a��c�ֱ�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ����aΪHԪ�ء�cΪFԪ�أ�bԭ�Ӻ��������Ϊ18-1-9=8����bΪOԪ�أ�d���������������Ľ�����������������ֳ�����̬����dΪFe���ݴ˽��
��� �⣺a��b��c��d��ԭ���������ε���������Ԫ�أ�a��b��c����Ԫ�ص�ԭ�Ӻ��������֮����Cl-�ĺ����������ȣ�a��c�ֱ�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ����aΪHԪ�ء�cΪFԪ�أ�bԭ�Ӻ��������Ϊ18-1-9=8����bΪOԪ�أ�d���������������Ľ�����������������ֳ�����̬����dΪFe��
A�����Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶O2-��F-��H-����H+������A����
B��a��c�γɻ�����ΪHF��HF��Һ����������跴Ӧ����ʴ���������ܱ����ڲ���ƿ�У���B����
C��Fe3+�Թ�������ķֽ��д����ã����ʱ�����������O2����C��ȷ��
D��Fe3+��������F-����D����
��ѡC��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ���ע��Ի���֪ʶ���������գ�ע��HF���ʵ������ԣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | -16Q kJ/mol | B�� | +8Q kJ/mol | C�� | +16 Q kJ/mol | D�� | -8 Q kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��ͼ�У����MnO2������Ũ����Ϳ�ȫ�������� | |
| B�� | ��ͼ�У���Ͳ�з����˼ӳɷ�Ӧ | |
| C�� | ��ͼ�У�������ɫ���� | |
| D�� | ��ͼ�У�ʪ�����ɫ��������ɫ����������Һ�����ձ��У�����Һ�����ԣ������Cl2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 B��
B�� C���״� D��CH3-O-CH3E��HO-CH2CH2-OH
C���״� D��CH3-O-CH3E��HO-CH2CH2-OH�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4+ | B�� | Ca2+ | C�� | Mg2+ | D�� | Al3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.01mol•L-1NH4Al��SO4��2��Һ��0.02mol•L-1Ba��OH��2��Һ�������ϣ�NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4��+Al��OH��3��+NH3•H2O | |
| B�� | һ�������£���0.5mol N2��g����1.5molH2��g�������ܱյ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6kJ•mol-1 | |
| C�� | ��ͼ��ʾH2��O2������Ӧ�����е������仯��H2��ȼ����Ϊ571.6 kJ•mol-1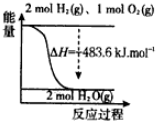 | |
| D�� | CO��g����ȼ������283.0 kJ•mol-1����CO2�ֽ���Ȼ�ѧ����ʽΪ��2CO2��g��=2CO��g��+O2��g����H=+283.0 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �±�Ϊ���ڱ��ж����ڵ�һ���֣���֪aԭ�ӵ������������ǵ�������������֮һ������˵������ȷ���ǣ�������
�±�Ϊ���ڱ��ж����ڵ�һ���֣���֪aԭ�ӵ������������ǵ�������������֮һ������˵������ȷ���ǣ�������| A�� | a������������Ӧˮ���������� | |
| B�� | b��d��ɵĻ����ﲻ����ˮ��Ӧ | |
| C�� | c�ĵ�������ǿ�Ӧ���������� | |
| D�� | c��d���γɹ��ۻ���������ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2-��-6-�һ�����
2-��-6-�һ����� 4��7��7-����-1-��ϩ
4��7��7-����-1-��ϩ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
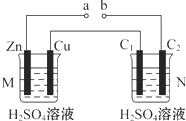
| A�� | a��b���ӣ�����һ��ʱ���װ��M����ҺpH���װ��N����ҺpH��С | |
| B�� | a��b���ӣ�װ��M������0.1 mol SO42-�Ƶ�Cu�缫��װ��N��C2���ų�H2 2.24 L����״���� | |
| C�� | a��bδ����ʱ��װ��N��C1�缫������������ | |
| D�� | ����a��b�Ƿ����ӣ�װ��M�й۲쵽��ʵ��������ͬ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com