
| A. | 用食醋清洗热水瓶中的水垢【主要成分是CaCO3和Mg(OH)2】 | |
| B. | 用煤气灶燃烧天然气为炒菜提供热量 | |
| C. | 烧菜用过的铁锅,经放置常出现红棕色斑迹 | |
| D. | 牛奶久置变质腐败 |
分析 氧化还原反应的特征是化合价的升降,从化合价变化的角度分析氧化还原反应,由此分析解答.
解答 解:A.食醋(CH3COOH)除去水瓶里的水垢[主要成分CaCO3和Mg(OH)2],发生复分解反应,没有元素化合价的变化,不是氧化还原反应,故A选;
B.液化石油气的燃烧属于氧化还原反应,故B不选;
C.烧菜用过的铁锅出现红棕色斑迹,属于铁被氧化为生锈的过程,故C不选;
D.牛奶久置变质腐败,为蛋白质被氧化的过程,为氧化还原反应,故D不选;
故选A.
点评 本题考查氧化还原反应,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意从元素化合价的角度认识相关概念,判断相关物质的性质,难度不大.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:解答题
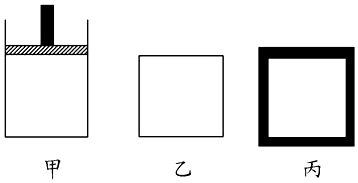
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
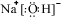 ,并指出其中存在的化学键.离子键和共价键
,并指出其中存在的化学键.离子键和共价键查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①⑤ | C. | ①②⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
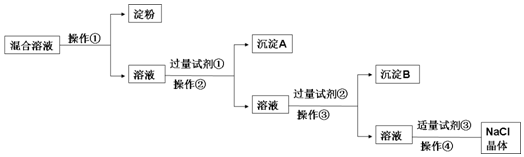
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了加快过滤速度,可用玻璃棒搅拌过滤器中的液体 | |
| B. | 在蒸馏时应先打开冷凝水开关,待水充满后再点燃酒精灯 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,然后换一个烧杯将上层液体放出 | |
| D. | 在做蒸馏实验时应将温度计的水银球浸没在液体里 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
对于相同物质的量的 SO2与SO3,下列说法正确的是
SO2与SO3,下列说法正确的是
A.硫元素的质量比为5:4 B.原子总数之比为4:3
C.质量之比为1:1 D.分子数之比为1:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是 ( )
A.MgO B.MgCO3 C.NaOH D.Mg(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com