
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子数多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1) D元素在周期表中的位置是___________,乙物质的电子式是___________。
(2) A、B、C、D、E五种元素的原子半径由小到大的顺序是_________(用元素符号填写)。
(3) E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是:____________________________。
(4)简述比较D与E金属性强弱的实验方法:_________________________。
【答案】第三周期第ⅡA族 ![]() O<N<Al<Mg<Na 2Al+2OH-+2H2O=2AlO-2+3H2↑ 镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应(其他合理也可)
O<N<Al<Mg<Na 2Al+2OH-+2H2O=2AlO-2+3H2↑ 镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应(其他合理也可)
【解析】
A、B、C、D、E都是短周期元素原子序数依次增大,C、B可按原子个数比2:1和1:1分別形成两种离子化台物甲和乙,则C为Na,B为O;A、B处于同一周期,且A原子的最外层电子数比次外层电子层多3个,则A为N元素,C、D、E同处另一周期,E是地壳中含量最高的金属元素,则E为Al,所以D为Mg。
(1)D为Mg,位于元素周期表中第三周期第ⅡA族,Na、O以1:1形成离子化合物乙,则乙为Na2O2,其电子式为:![]() ;
;
(2)电子层越多,半径越大,同周期从左向右原子半径在减小,则原子半径为O<N<Al<Mg<Na;
(3)C的最高价氧化物对应的水化物的溶液为NaOH,与A反应的离子反应为2Al+2OH-+2H2O=2AlO-2+3H2↑;
(4)根据金属与热水的反应可确定金属的活泼性,则设计实验为镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应,故本题正确答案是:镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应(其他合理也可)。


科目:高中化学 来源: 题型:
【题目】A—E为常见的有机物。以A为原料合成化合物E,其合成路线如图1所示。已知:A的产量通常用来衡量一个国家的石油化工水平;2CH3CHO+O2![]() 2CH3COOH。
2CH3COOH。
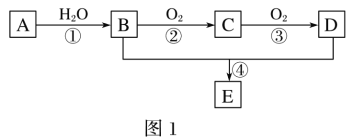
(1)A的分子式______。
(2)A中官能团的名称是_____;B中官能团的结构简式是_____。
(3)反应①的反应类型为_____;反应④的反应类型为_____。
(4)反应④的化学方程式为_____。
(5)某学习小组设计B催化氧化的实验装置如图,根据图2装置回答问题。
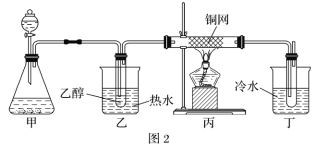
①装置甲锥形瓶中盛放的固体为过氧化钠,请写出甲中反应的化学方程式_____。
②B催化氧化的产物与葡萄糖具有相同的特征反应,将所得的氧化产物滴加到新制氢氧化铜悬浊液中加热,现象为_____。
③实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
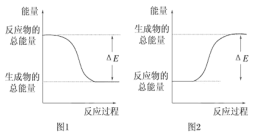
【题目】(一)下列反应中,能量变化符合图 1 的有____ (填序号,下同),符合图 2 的有______。
①煅烧石灰石 ②木炭燃烧 ③炸药爆炸 ④酸碱中和 ⑤碳与二氧化碳高温反应 ⑥食物因氧化而腐败
(二)为了探究化学能与热能的转化,某实验小组设计了如下图(I、II、III)三套实验装置:
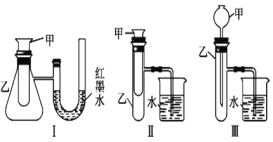
(1)某同学选用装置I进行实验(实验前 U 形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U 形管中可观察到的现象是________。
(2)为探究固体 M 溶于水的热效应,选择装置II进行实验(反应在甲中进行)。
①观察到烧杯里产生气泡,则可推出 M 溶于水___是放热反应(填“一定”或“可能” ),理由是_______;
②若观察到烧杯里的玻璃管内形成一段水柱,则 M 可能是____________。
(3)至少有两种实验方法能证明超氧化钾与水的反应(4KO2+2H2O=4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择上述装置____(填 “I”或“III”)进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到棉花燃烧,则说明该反应是______反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:
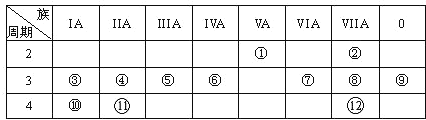
(1)写出下列元素符号:①______ ,⑥______,⑦______。
(2)画出原子的结构示意图:④________________,⑧_________________。
(3)在①~![]() 元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是_______(均填元素名称)。
元素中,金属性最强的元素是_____,非金属性最强的元素是______,最不活泼的元素是_______(均填元素名称)。
(4)元素③、⑩、![]() 的氢氧化物碱性由强到弱的顺序________________;元素⑥、⑦、⑧的氢化物稳定性由弱到强的顺序______________________(均用化学式填空)。
的氢氧化物碱性由强到弱的顺序________________;元素⑥、⑦、⑧的氢化物稳定性由弱到强的顺序______________________(均用化学式填空)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是

A. a为负极,是铁片,烧杯中的溶液为硫酸
B. b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C. a为正极,是碳棒,烧杯中的溶液为硫酸
D. b为正极,是碳棒,烧杯中的溶液为硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
第二周期 | ① | ② | ③ | |||||
第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
第四周期 | ⑩ |
(1)在这些元素中,化学性质最活泼的是___;化学性质最不活泼的是___(填元素符号)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子___,④和⑧结合的化合物的电子式是___,该化合物属于___化合物(填“共价”或“离子”)。
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是___(用化学式表示),⑥、⑦、⑧三种元素的非金属性逐渐___,①、④、⑩三种元素原子还原性逐渐___(填“增强”或“减弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)制硫酸的三种原料是___、___、___,三个生产过程是①___,写出反应方程式___,②___,写出反应方程式___,③___,写出反应方程式__,三废指的是____、___、___。
(2)合成氨的反应原理工业合成氨的反应条件为浓度使用过量的___、温度___℃、高压__MPa、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )
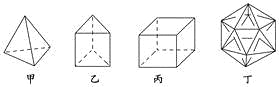
A. 1 mol甲分子内含有10 mol共价键
B. 由乙分子构成的物质不能发生氧化反应
C. 丙分子的二氯取代产物只有三种
D. 分子丁是不可能合成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
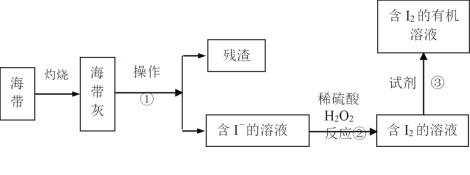
(1)操作①的名称是_________;反应②的离子方程式是____________,
(2)下述物质中可做试剂③的是_______。
A.乙醇 B.苯 C.乙酸 D.四氯化碳
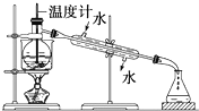
(3)从含I2的有机溶液中提取碘和回收有机溶剂(碘的沸点为184℃,该有机溶剂的沸点为77℃),需要经过蒸馏,指出下面蒸馏装置图的错误之处(其中一处即可):______。纠正错误后再进行蒸馏操作,最后晶体I2在________里聚集。
(Ⅱ)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g)![]() 2NH3(g)。
2NH3(g)。
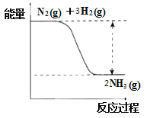
(4)合成氨的反应中的能量变化如下图所示。该反应是_________反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量_________(填“大于”或“小于”)生成物化学键形成放出的总能量。
(5)在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是___(填序号)。
A.容器中N2 、H2 、NH3共存
B.N2、NH3浓度相等
C. N2、H2、NH3的物质的量之比为1:3:2
D.容器中的压强不随时间变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com