
下列实验设计能够成功的是( )
A.检验亚硫酸钠试样是否变质:试样 滴加
滴加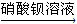 白色沉淀滴加
白色沉淀滴加 沉淀不溶解-→说明试样已变质
沉淀不溶解-→说明试样已变质
B.除去粗盐中硫酸钙杂质:粗盐 足量
足量 足量
足量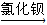 溶液
溶液 滤液中
滤液中 盐酸
盐酸 精盐
精盐
C.检验某溶液中是否含有Fe2+试样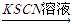 溶液颜色无变化
溶液颜色无变化 溶液变红色-→溶液中含有Fe2+
溶液变红色-→溶液中含有Fe2+
D.证明酸性条件H2O2的氧化性比I2强:NaI溶液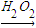 稀硝酸
稀硝酸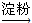 溶液变蓝色-→氧化性:H2O2>I2
溶液变蓝色-→氧化性:H2O2>I2
科目:高中化学 来源:2015-2016学年江西省等四校高一下第二次月考化学试卷(解析版) 题型:选择题
设NA 代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
A.标准状况下,2.24L戊烷所含分子数为0.1 NA
B.乙烯和环丙烷(C3H6)组成的28g混合气体中含有4NA 个氢原子
C.17.6g丙烷中所含的极性共价键为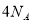 个
个
D.常温常压下,22.4L乙烯中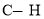 键数为4
键数为4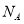
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三最后一卷理综化学试卷(解析版) 题型:填空题
“关爱生命,注意安全”。惨痛的天津爆炸触目惊心,火灾之后依然火势绵延不绝的原因之一是易燃物中含有电石。工业上常用电石(主要成分为CaC2,杂质为CaS等)与水反应生产乙炔气。
(1)工业上合成CaC2主要采用氧热法。
已知:CaO(s)+3C(s)=CaC2(s)+CO(g) △H=+464.1kJ·mol-1
C(s)+l/2O2(g)=CO(g) △H=-110.5kJ.mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO,为维持热平衡,每生产l molCaC2,转移电子的物质的量为_______。
(2)已知2000℃时,合成碳化钙的过程中还可能涉及到如下反应
CaO(s)+C(s)  Ca(g)+CO(g) K1 △H1=a KJ·mol-1
Ca(g)+CO(g) K1 △H1=a KJ·mol-1
Ca(g)+2C(s)  CaC2(s) K2 △H2=b KJ·mol-1
CaC2(s) K2 △H2=b KJ·mol-1
2CaO(s)+CaC2(s)  3Ca(g)+2CO(g) K3 △H3=c KJ·mol-1
3Ca(g)+2CO(g) K3 △H3=c KJ·mol-1
则K1=_______ (用含K2、K3的代数式表示);c=_____(用含a、b的代数式表示)。
(3)利用电石产生乙炔气的过程中产生的H2S气体制取H2,既廉价又环保。
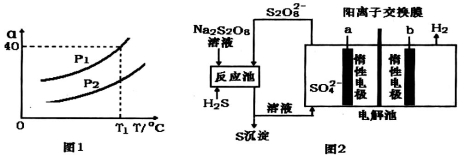
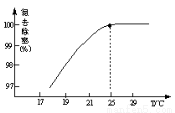
①利用硫化氢的热不稳定性制取氢气。在体积为2L的恒容密闭容器中,H2S起始物质的量为2mol,达到平衡后H2S的转化率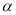 随温度和压强变化如图l所示。据图计算T1℃时压强P1时,硫为气态,则平衡体系中H2的体积分数_____。由图知压强P1__P2(填“大于”“小于”或“等于”),理由是______。
随温度和压强变化如图l所示。据图计算T1℃时压强P1时,硫为气态,则平衡体系中H2的体积分数_____。由图知压强P1__P2(填“大于”“小于”或“等于”),理由是______。
②电化学法制取氢气的原理如图2,请写出反应池中发生反应的离子方程式_____,惰性电极a上发生的电极反应式为_______。
查看答案和解析>>
科目:高中化学 来源:2016届陕西西藏民族学院附中高三下考前三模理综化学试卷(解析版) 题型:选择题
某有机物的结构简式为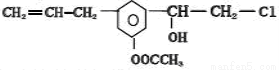 ,关于它的说法正确的是( )
,关于它的说法正确的是( )
A.该物质属于芳香烃
B.该物质易溶于水
C.1mol该物质最多能与2mol NaOH反应
D.该物质能发生的反应类型有加成、水解、消去、氧化
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮复习训练六化学试卷(解析版) 题型:实验题
S2Cl2是一种金黄色易挥发的液体,常用作橡胶硫化剂.某化学兴趣小组 拟设计实验制备少量的S2Cl2,査阅资料知S2Cl2在水中易发生歧化反应(一部分硫元素化 合价升高,另一部分化合价降低).加热条件下硫单质和干燥、纯净的Cl2反应即可生成S2Cl2,反应的化学方程式为:2S+Cl2 S2Cl2.
S2Cl2.
反应涉及的几种物质的熔沸点如下:
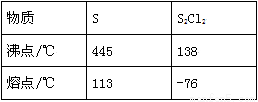
该小组设计的制备装置如图(夹持仪器已略去)。
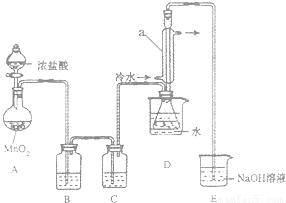
回答下列问题:
(1)连接好实验装置后的第一步实验操作是_____________;
(2)实验中需要加热的仪器是_____________(填写字母)
(3)装置B、C中的试剂分别是_____________;
(4)装置D中仪器a的作用是_____________;
(5)反应结束后从锥形瓶内混合物中分离出产品的方法是_____________;
(6)若实验过程中缺少C装置,发现产品浑浊不清,请用化学方程式表示其原因_____________;
(7)实验完毕,小组中的一位同学把剩余浓盐酸倒入E烧杯中,发现有黄绿色剌激性气 体产生.用离子方程式表示产生该现象的原因_____________。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前周练模拟化学试卷(解析版) 题型:填空题
氮可以形成多种化合物,如NH3、N2H4、NH4NO3、NF3等。
(1)已知:N2(g)+2H2(g)═N2H4(l)△H=+50.6kJ•mol-1
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
则N2H4(l)+O2(g)═N2(g)+2H2O △H= _________kJ•mol-1;
(2)污水中的NH4+可以用氧化镁处理,发生如下反应:
MgO+H2O Mg(OH)2 Mg(OH)2+2NH4+
Mg(OH)2 Mg(OH)2+2NH4+ Mg2++2NH3•H2O
Mg2++2NH3•H2O
①温度对氮处理率的影响如图所示.在25℃前,升高温度氮去除率增大的原因是________________;
②剩余的氧化镁,不会对废水形成二次污染,理由是________________;
(3)污水中的含氮化合物,通常先用生物膜脱氮工艺进行处理在硝化细菌的作用下将NH4+氧化为NO3-(2NH4++3O2═2HNO2+2H2O+2H+;2HNO2+O2=2HNO3).然后加入甲醇,甲醇和NO3-反应转化为两种无毒气体.
①上述方法中,14g铵态氮元素转化为硝态氮元素时需氧的质量为_______g。
②写出加入甲醇后反应的离子方程式________________;
(4)使用NaBH4为诱导剂,可使Co2+与肼在碱性条件下发生反应,制得高纯度纳米钴,该过程不产生有毒气体。
①写出该反应的离子方程式________________;
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如下图1所示,则N2H4发生分解反应的化学方程式为________________;
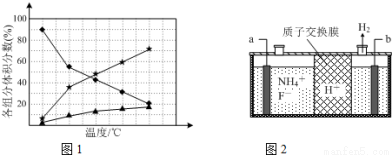
(5)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如上图2所示。写出a电极的电极反应式__________________。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前周练模拟化学试卷(解析版) 题型:选择题
下列图示与对应说法正确的是
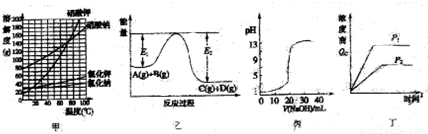
A.图甲表明利用NaNO3和KCl可能制取KNO3和NaCl
B.图乙表明反应A(g)+B(g)=C(g)+D(g)焓变大于零
C.图丙表示用0.1mol/LNaOH溶液滴定20mL0.1mol/L硫酸时混合溶液pH变化情况
D.图丁表示一定温度下反应N2(g)+3H2(g) 2NH3(g)在不同压强时浓度商(Qc)变化情况
2NH3(g)在不同压强时浓度商(Qc)变化情况
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北市高一5月月考化学试卷(解析版) 题型:选择题
下列各组物质中,不管它们以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳的量不变的是
A.乙烷和苯 B.乙醇和丙醇
C.乙醇和乙醚 D.甲醛(HCHO)和乙酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高一下6月考化学卷(解析版) 题型:选择题
按系统命名法下列名称不正确的是( )
A.1一甲基丙烷 B.2一甲基丙烷
C.2,2一二甲基丙烷 D.3一乙基庚烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com