
已知反应:
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3,
下列说法正确的是( )
A. 上述三个反应都有单质生成,所以都是置换反应
B. 反应③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
C. 反应②中还原剂与氧化剂的物质的量之比为6:1
D. 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:选择题
向MgSO4和Al2(SO4)3的混合溶液中, 逐滴加入NaOH溶液。下列图象中(横坐标表示NaOH溶液的体积, 纵坐标表示沉淀质量), 能正确表示上述反应的是 ( )
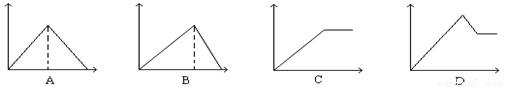
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二2月月考化学试卷(解析版) 题型:选择题
在一定条件下发生反应:2A(g)+2B(g) xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L•min),下列说法正确的是( )
xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L•min),下列说法正确的是( )
A. A和B的转化率均是20% B. x=4
C. 平衡时A的物质的量为2.8mol D. 平衡时气体压强比原来减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市高一下学期选拔考试化学试卷(解析版) 题型:实验题
如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)
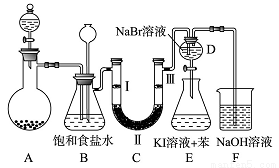
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的离子反应方程式为:_____________.装置 B 中饱和食盐水的作用是_________________;
若C处发生了堵塞,则B中的现象为__________________.
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ应该依次放入____(填编号)
① | ② | ③ | ④ | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为______色,说明 ________________;打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是__________________;
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为_____.
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用的漂白液,同时有 NaHCO3 生成,该反应的化学方程式是______.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市高一下学期选拔考试化学试卷(解析版) 题型:选择题
下列对实验现象的预测不正确的是( )
A. 向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入过量NaOH溶液,溶液又变浑浊
B. 向氢氧化铁胶体中滴加盐酸至过量,开始有沉淀出现,后来沉淀又溶解
C. 向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去
D. 向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省葫芦岛市高一下学期选拔考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 1mol FeI2与足量氯气反应时转移的电子数为2NA
B. 2L 0.5mol•L﹣1硫酸钾溶液中阴离子所带电荷数为NA
C. 1mol Na2O2固体中含离子总数为4NA
D. 22gCO2与标准状况下11.2LHCl所含的分子数相同
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:简答题
七铝十二钙是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
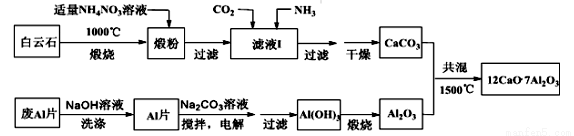
(1)煅粉主要含__________,该工艺中不能用(NH4)2SO4代替NH4NO3,原因是_________。
(2)滤液I中主要的阴离子有_________;若滤液I中仅通入CO2,会生成________,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为______________。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为_______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省凯里市高二下学期开学考试理综化学试卷(解析版) 题型:简答题
铜是人类最早使用的金属之一,中国使用铜的历史年代久远。大约在六、七千年以前中国人的祖先就发现并开始使用铜。纯铜是柔软的金属,呈紫红色,延展性好,导热性和导电性高,因此在电缆和电气、电子元件是最常用的材料,请回答下列问题:
(1)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_______(填选项字母)
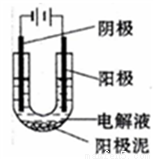
a.粗铜接电源正极,发生氧化反应
b.溶液中Cu2+向阴极移动
c.电解过程中,阳极和阴极的质量变化相等
d.利用阳极泥可回收Al、Zn等金属
(2)目前的电路板,主要由线路和图面组成,线路是作为原件之间导通的工具,在设计上会另外设计大铜面作为接地及电源层,在印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为______________。
(3) Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快变蓝色,试写出该反应的离子方程式___________________。
(4)Cu2O中的Cu+不稳定,向Cu2O滴加稀硫酸,有紫红色物质生成,溶液变为蓝色,写出反应的离子方程式_________________。
(5)火法炼铜的原理:Cu2+O2 2Cu+SO2,在改反应中每生成1molCu,转移________mole-。
2Cu+SO2,在改反应中每生成1molCu,转移________mole-。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三下学期开学考试化学试卷(解析版) 题型:选择题
下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
表述Ⅰ | 表述Ⅱ | |
A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1—与Na+间的作用力大于碘晶体中分子间的作用力 |
B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
C | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com